Mejora de la calidad en el preanálisis de la Unidad Técnica de Patología Clínica
Mejora de la calidad en el preanálisis de la Unidad Técnica de Patología Clínica |
INTRODUCCIÓN. El preanálisis es un proceso en el que se presenta el 71,0% de errores en el laboratorio clínico, por la presencia de factores como: la falta de automatización y la intervención de personal propio y ajeno al servicio, que lo convierte en vulnerable. OBJETIVO. Identificar, definir y estandarizar sub procesos preanalíticos en base a la norma ISO 15189:2012, identificar y realizar pilotaje de la aplicación de indicadores armonizados como elementos de mejora continua de la calidad. MATERIALES Y MÉTODOS. Estudio de tipo observacional, descriptivo en el que se identificó el proceso preanalítico actual y sus sub procesos; se los estandarizó previo a un pilotaje, definiendo los indicadores para su aplicación en la Unidad Técnica de Patología Clínica del Hospital de Especialidades Carlos Andrade Marín de la ciudad de Quito, Ecuador en el periodo junio a diciembre de 2018. RESULTADOS. Los sub procesos preanalíticos estandarizados fueron: Atención al Usuario, Identificación y generación de códigos, Toma de muestras, Transporte, preservación interna, separación y distribución de muestras; y, Referencia y contra referencia con sus procedimientos correspondientes y el tablero de indicadores. CONCLUSIÓN. Utilizar la norma de acreditación ISO15189:2012 para identificar y estandarizar sub procesos del proceso preanalítico, permitirá la mejora continua de la gestión de la calidad del laboratorio hospitalario de alta complejidad en su nivel de productividad.
Palabras Clave: Gestión de la Calidad; Fase Preanalítica; Control de Calidad; Normas; Algoritmos; Indicadores (Estadística); Laboratorios.
INTRODUCTION. Pre-analysis is a process where 71,0% of errors made in the clinical laboratory, due to the existence of factors such as: lack of automation and intervention of own personnel and other personnel non-related to the service, which
render the process vulnerable. OBJECTIVE: To identify, define and standardize preanalytic sub processes, based on ISO 15189:2012 standard, identify and pilot the
application of harmonized indicators as elements of continuous quality improvement.
MATERIALS AND METHODS. Observational-descriptive study where the current
preanalytical process and its sub processes were identified; they were standardized
prior to piloting, defining the indicators in the Clinical Pathology Technical Unit of
the Hospital de Especialidades Carlos Andrade Marín of the city Quito, Ecuador in
the period from June to December 2018. RESULTS. The standardized pre-analytic
processes were: Customer service, Identification and generation of codes, Sampling,
Transportation Internal preservation, separation and distribution of samples; and, Reference and counter reference with their corresponding procedures and the indicator
board. CONCLUSION. To use the accreditation standard ISO15189:2012 to identify
and standardize pre-analytic sub-processes, will allow the continuous improvement
of the quality management of the hospital laboratory of high complexity in its level or productivity.
Keywords: Quality Management; Pre-Analytical Phase; Quality Control; Standards; Algorithms; Indicators (Statistics); Laboratories.
El laboratorio clínico juega un rol importante en la toma de decisiones médicas respecto al paciente mediante la información que este emite a través de sus resultados oportunos para su interpretación, que lo compromete a mantener un continuo control para la detección y evitar posibles desviaciones, errores o incidencias en cada uno de sus procesos, principalmente en el proceso conocido como preanálisis1.
La norma ISO 15189:2012 identifica varios requisitos que van a permitir controlar la trazabilidad de las muestras que se ven afectadas por varios factores desde la generación de la orden médica que no solo involucran al personal, hasta el almacenamiento de la muestra previo al análisis, mediante la generación de documentación, registros e indicadores necesarios para poder implementar acciones preventivas, correctivas o de mejora2.
Los tipos de errores detectados en los laboratorios clínicos son: de bajo impacto (detectado a tiempo dentro del proceso, se soluciona repitiendo el proceso), mediano impacto (no detectado a tiempo, ligeras consecuencias para el paciente) y de alto impacto (después de haber sufrido consecuencias severas)3.
Los errores que se presentan con mayor frecuencia se resumen en la Tabla 1, estos suelen ser de bajo impacto para el paciente pero independientemente del tipo de error, estos proporcionan oportunidades de aprendizaje así como en la habilidad de localizar debilidades de los diferentes sub procesos y procedimientos que puedan afectar la trazabilidad de las muestras4.
Para la minimización de errores y control de las diferentes actividades que influyen en el preanálisis, se puede contar con la ayuda de requisitos establecidos en la norma de acreditación internacional ISO 15189:2012 “Laboratorios Clínicos-Requisitos Particulares para la Calidad y la Competencia”, que permiten evidenciar que el Laboratorio Clínico posee un sistema de gestión de calidad y competencia técnica, además con esta, se puede incrementar la productividad del Servicio con la mejora de los procesos operativos, permitir estandarizar metodologías, reducir costos a nivel del Servicio, de fallos y riegos que pueden poner en duda su calidad y la seguridad de los pacientes5-8. Al utilizar los requerimientos de la norma ISO 15189:2012, se garantiza que las diferentes actividades, no causarán ningún efecto contraproducente en: a) trazabilidad de muestras primarias, b) resultados obtenidos del proceso analítico e c) interpretación de resultados.
Variables |
Sub Proceso Preanalítico |
Tipos de errores |
||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Fuente. Base de datos de la investigación. Elaborado por. Autores | ||||||||||
Pacientes |
Solicitud de Pruebas |
-Solicitud indiscriminada de pruebas innecesarias |
||||||||
Identificación del paciente |
- Ingreso de información incompleta - Ingreso de información errónea - Identificación erronea de muestras |
|||||||||
Muestras |
Extracción sanguinea y recogida de muestras |
- Ausencia de condiciones preanalíticas por parte del paciente - Posición incorrecta del paciente - Orden inadecuado de llenado de tubos - Contaminación de muestras biológicas - Presencias de Hemólisis - Presencias de coágulos - Volúmenes insuficientes - Contenedores inadecuados - Ausencia de registros de hora de la flebotomía. |
||||||||
Ingreso de dtos en el lab. clínico |
- Fallo humano en el ingreso de las solicitudes |
|||||||||
Conservación de las muestras |
- Transporte en contenedores y a temperaturas inadecuados - Ausencia de registros de tiempos de la llegada de muestras |
|||||||||
El monitoreo a través de indicadores permite localizar los posibles desvíos que pueden darse en las actividades de dicho proceso. Los indicadores, se han clasificado en dos grupos: los que tienen relación con problemas en la identificación del paciente y los que tienen relación con la presencia de problemas en las muestras. Existen programas de indicadores de calidad desarrollados e implementados a nivel mundial, como el desarrollado por el Grupo de Trabajo de “Errores de Laboratorio y Seguridad del Paciente” (WG-LEPS) de la Federación Internacional de Química Clínica (IFCC) o por el Grupo de Trabajo para la Fase Preanalítica (WG-PRE) de la Federación Europea de Química Clínica y Medicina del Laboratorio9-13. El WG-LEPS de la IFCC maneja la clasificación de indicadores de calidad tradicional e incluye aquellos que detectan problemas en las peticiones analíticas, estos proyectos buscan llegar a la armonización / estandarización en el uso y manejo de dichas herramientas de calidad para conseguir una comparación oportuna entre laboratorios con respecto al manejo del preanálisis14-18.
El presente estudio fue de tipo observacional, descriptivo, no se seleccionó universo ni muestra, ni criterios de inclusión y exclusión, ya que se trabajó en gestión, relacionada a la identificación, definición y estandarización de sub procesos del proceso preanalítico de la Unidad Técnica de Patología Clínica (UTPC) en el Hospital de Especialidades Carlos Andrade Marín (HECAM), en el periodo de junio a diciembre de 2018. Para la identificación de actividades actuales, elaboración documental, matriz de marco lógico se utilizó el programa Microsoft Word. Con un check list de la norma ISO 15189:2012 apartado 5.4, permitió identificar la brecha entre los sub procesos actuales cumplidos y por cumplir pertenecientes al proceso del preanálisis; y, se realizó su estandarización, con la misión, el alcance, los involucrados, actividades críticas, flujogramas, fichas, y los procedimientos correspondientes a cada uno de los sub procesos. La diagramación de los flujogramas fue con Bizagi Modeler; se aplicó fichas para el registro de sub procesos; se formuló el tablero de indicadores; y para el análisis de datos preanalíticos, se aplicó Microsoft Excel.
Los indicadores de calidad preanalíticos se completaron acorde a la norma ISO 15189:2012 y WG-LEPS de la IFCC; se capacitó al personal de la UTPC involucrado en el proceso preanalítico tanto en los Servicios de Consulta Externa, Hospitalización y Emergencia.
Se detectó una brecha de 48,0% (24;50) de cumplimiento de requerimientos preanalíticos descritos en la norma ISO 15189:2012. Tabla 2.
Se logró estandarizar cinco sub procesos preanalíticos, que se enumeran en la Tabla 3, presentaron cierto grado de complejidad debido a la influencia directa de factores como: falta de infraestructura, automatización y la intervención de personal propio y ajeno al servicio.
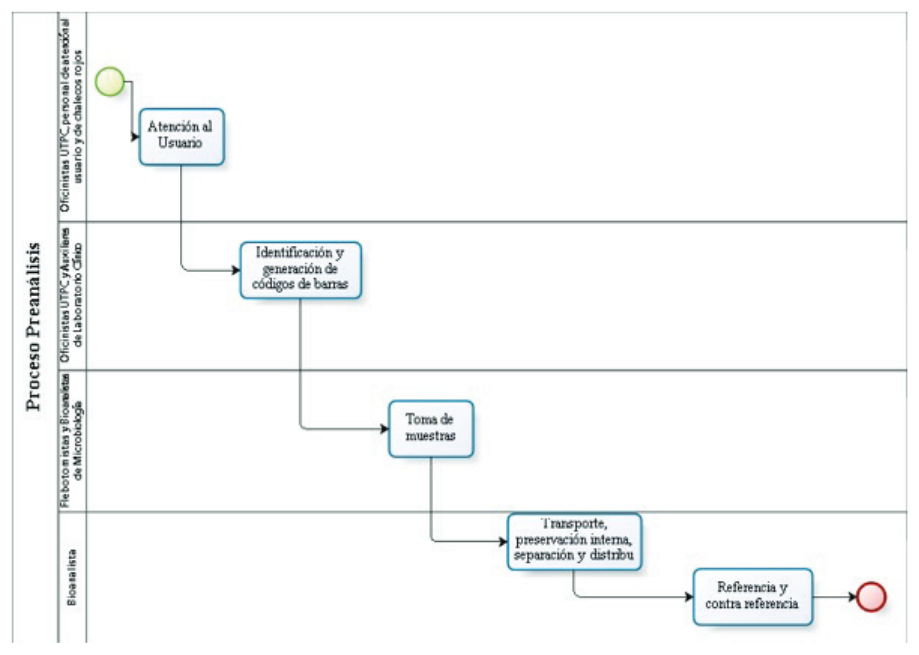
Se esquematiza el flujograma de los cinco sub procesos del proceso preanalítico estandarizado. Figura 1.
Al identificar las actividades de los sub procesos preanalíticos se elaboraron diez procedimientos técnicos acordes a los requisitos de la norma ISO 15189:2012, los cuales se enumeran en la Tabla 4.
Se estableció cuarenta indicadores para el monitoreo piloto del proceso preanalítico, los pre existentes fueron el 63,0% (25;40) y los estandarizados 37,0% (15;40). Tabla 5.
Para el monitoreo piloto de los sub procesos en la UTPC se tomó los indicadores más representativos del preanálisis:
En el sub proceso de Atención al Usuario se monitoreó el indicador % Vía por la que el usuario conoció el agendamiento; y, con un seguimiento de 5 meses, periodo mayo a septiembre de 2018, en el Servicio de Consulta Externa; se apreció que los usuarios lo conocieron a través del médico tratante.
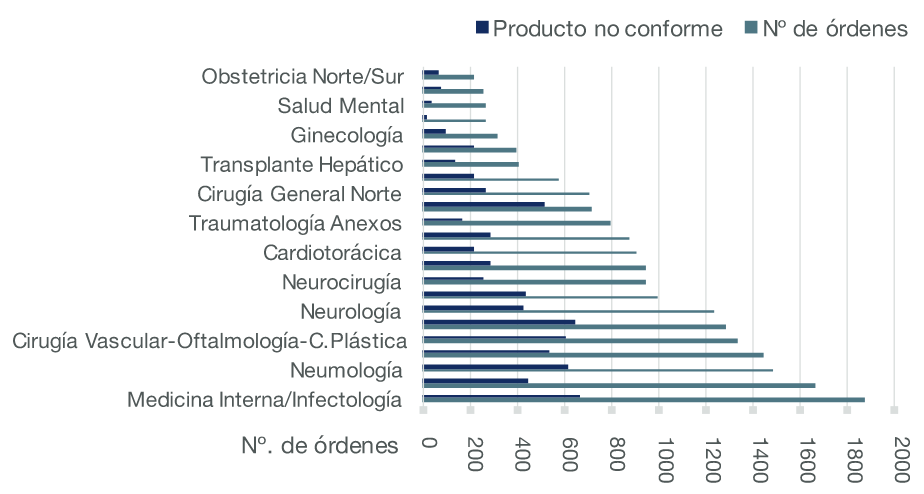
En el sub proceso Identificación y generación de códigos de barras se monitoreó el indicador # De órdenes de hospitalización no conformes por servicio; y, con un seguimiento de 8 meses, periodo marzo a octubre de 2018, se detectó que Medicina Interna / Infectología fue el Servicio que emitió el mayor número de órdenes y a su vez presentó el mayor número de no conformidades en las órdenes. Figura 2.
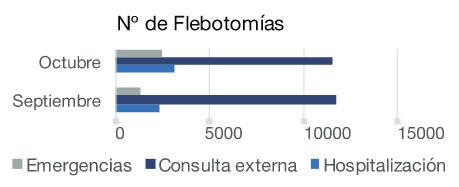
En el sub proceso de Toma de muestras se monitoreó el indicador # Total de flebotomías realizadas en toda la UTPC, en septiembre y octubre de 2018, se determinó un total de 16298 flebotomías, de las cuales corresponden: 11,6% (1892;16298) a Emergencias, 71,5% (11657;16298) a Consulta Externa y 16,8% (2749;16298) a Hospitalización. Figura 3.
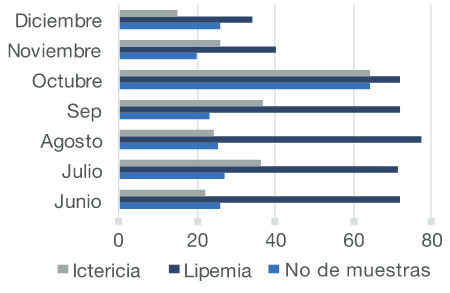
En el sub proceso Transporte, preservación interna, separación y distribución de muestras se monitoreó el indicador # Muestras de sangre no conformes (ictéricas, hemolisadas y lipémicas); y, con un seguimiento de 7 meses, periodo de junio a diciembre de 2018 en el Área de Química Clínica; se obtuvieron 125 muestras de sangre no conformes: 26,0% (32;125) de muestras ictéricas, 50,0% (63;125) de muestras lipémicas y 24,0% (30;125) de muestras hemolisadas. Figura 4.
En el sub proceso Referencia y contra referencia de muestras se identificó elementos críticos con relación a las condiciones en las que estas fueron referidas a la UTPC: muestras no etiquetadas, contenedores inadecuados, mal transportadas o inexistentes, lo que permitió generar los formatos necesarios para garantizar la trazabilidad de las muestras.
De la brecha de cumplimiento de requerimientos preanalíticos de la norma ISO 15189:2012, el apartado que presentó complejidad para su cumplimiento en el estudio fue el 5.4.2, ya que la UTPC debía prestar más atención en la información que se le proporciona a los pacientes y usuarios pero esta actividad se encuentra a cargo no solo del personal de la Unidad, esta también es llevada a cabo por personal externo, al cual no se le proporciona la capacitación necesaria o por la presencia de rotación constante2,18.
La norma ISO 15189:2012 dio los requerimientos que la UTPC debía cumplir en el proceso preanalítico, enfocándose en un modelo de gestión preventivo y pro activo al permitir que nos preocupemos en cómo aplicar dichos requerimientos a través de la identificación, definición y estandarización de los sub procesos preanalíticos al considerar la cantidad de actividades realizadas en el Servicio relacionadas a su nivel de complejidad, el volumen y tipo de muestras manejadas; y, la cantidad de personal con el que cuenta6,19.
Los flujogramas desarrollados fueron parte de la definición de los sub procesos preanalíticos, así el flujograma presentado es un ejemplo en relación a los elaborados para cada sub proceso estandarizado, cabe recalcar que ciertos sub procesos cuentan con más de un flujograma por presentar variaciones según en el Servicio de la UTPC que se aplique. Además para minimizar errores localizados fue necesario que todos los procedimientos técnicos fueran descritos minuciosamente para no dejar espacio a la subjetividad de estos y poder cumplir con todos los apartados de la norma ISO 15189:20128,19.
Los indicadores preanalíticos no deben ser seleccionados de manera indiscriminada para formar el tablero de indicadores, se debe establecer criterios de selección como: la realidad del Laboratorio, la existencia de indicadores armonizados/estandarizado y la facilidad de medición12,13,20.
Los indicadores más representativos de los sub procesos preanalíticos, pudieron ser medidos en el monitoreo piloto gracias al compromiso del personal que participó en la recolección y condensación de información a través de los registros propuestos.
La técnica de observación directa y definición de actividades fue de gran utilidad en la identificación de los sub procesos preanalíticos actuales de la Unidad Técnica de Patología Clínica ya que permitió manejar diferentes eventos tal y como se manifestaban en sus escenarios naturales, a través de la identificación de nodos vulnerables de duplicidad de actividades de las personas involucradas y también permitió establecer de mejor manera la brecha existente entre las mismas.
Utilizar la norma ISO15189:2012, facilitó identificar los sub procesos actuales del proceso de la fase preanalítica, al elaborar los flujogramas y procedimientos, permitió integrar las diferentes actividades, el cierre de la brecha existente entre las mismas e identificar y construir el tablero de indicadores. Además al establecer la estandarización del proceso preanalítico, permitirá la mejora continua de la gestión de la calidad del laboratorio hospitalario de alta complejidad en su nivel de productividad.
Socializar el proceso preanalítico estandarizado al personal involucrado, que se estableció para la Unidad Técnica de Patología Clínica.
Implementar la mejora continua de la calidad que le permita mejorar el desempeño del Servicio en beneficio del usuario.
UTPC: Unidad Técnica de Patología Clínica; HECAM: Hospital de Especialidades Carlos Andrade Marín, WG-LEPS: Grupo de Trabajo de “Errores de Laboratorio y Seguridad del Paciente; IFCC: Federación Internacional de Química Clínica; WG-PRE: Grupo de Trabajo para la Fase Preanalítica.
LV, JE: concepción y diseño del trabajo, análisis de resultados, redacción del manuscrito, revisión crítica del manuscrito, aprobación de su versión final. TA: recolección de datos y obtención de información condesada, análisis de resultados. Todos los autores leyeron y aprobaron la versión final del artículo.
Lenin Ramiro Villalta Guzmán. Doctor en Medicina y Cirugía, Médico Especialista en Patología Clínica, Magister en Sistemas de Gestión de Calidad, Universidad Central del Ecuador, Médico Coordinador del Área de Calidad, Unidad Técnica de Patología Clínica, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID ID: https://orcid.org/0000-0003-0891-8644
Jhoselyn Alexandra Escobar Morejón. Estudiante de Bioquímica Clínica, Pontificia Universidad Católica del Ecuador. Unidad Técnica de Patología Clínica, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID ID: https://orcid.org/0000-0002-0901-8712
Tatiana Isabel Andrade Barreno. Licenciada en Laboratorio Clínico, Universidad Central del Ecuador. Unidad Técnica de Patología Clínica, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID ID: https://orcid.org/0000-0001-5996-7521
Se utilizaron recursos bibliográficos de uso libre, la información recolectada está disponible bajo requisición al autor principal.
El artículo científico fue aprobado por pares y por el Comité de Ética de Investigación en Seres Humanos – CEISH/ HECAM.
La publicación fue aprobada por el Consejo Editorial del HECAM.
El trabajo se realizó con recursos propios de los autores.
Los autores reportaron no tener ningún conflicto de interés, personal, financiero, intelectual, económico y de interés corporativo.
Un agradecimiento fraterno a todo el personal de salud y administrativo de la Unidad Técnica de Patología Clínica del Hospital de Especialidades Carlos Andrade Marín.