Respuesta a diferentes escenarios y complicaciones hematológicas en COVID-19.
Respuesta a diferentes escenarios y complicaciones hematológicas en COVID-19. |
Respuesta a diferentes escenarios y complicaciones hematológicas en COVID-19.
Response to different scenarios and hematological complications in COVID-19.
Andrés Orquera Carranco1, Paola María Velasco Maldonado2, Manuel Antonio Granja Morán1, Mauricio Rodrigo Heredia Fuenmayor1 María Fernanda Luján Jiménez1 Miriam Muñoz Guerra1 José Isidro Páez Espín1 Grace Paulina Salazar Vega1 Erwin Bolívar Sánchez Paz1 Julia Edith Soria Silva1 Paulina del Rosario Vásconez Conrado1
Dr. Juan Dante Páez Moreno, Gerente General HECAM.
Dr. Miguel Ángel Moreira, Director Técnico HECAM.
Fecha: 2020-04-24
Código: HCAM- SGC-HM-PR-002
Andrés Orquera Carranco, Unidad Técnica de Hematología HECAM.
Paola María Velasco Maldonado, Unidad Técnica de Hematología HECAM.
Manuel Antonio Granja Morán, Unidad Técnica de Hematología HECAM.
Mauricio Rodrigo Heredia Fuenmayor, Unidad Técnica de Hematología HECAM.
María Fernanda Luján Jiménez, Unidad Técnica de Hematología HECAM.
Miriam Muñoz Guerra, Unidad Técnica de Hematología HECAM.
José Isidro Paéz Espín, Unidad Técnica de Hematología HECAM.
Grace Paulina Salazar Vega, Unidad Técnica de Hematología HECAM.
Erwin Bolívar Sánchez Paz, Unidad Técnica de Hematología HECAM.
Julia Edith Soria Silva, Unidad Técnica de Hematología HECAM.
Paulina del Rosario Vásconez Conrado, Unidad Técnica de Hematología. HECAM.
Dr. Juan Dante Páez Moreno. Comité de Farmacia y Terapéutica HECAM.
Dra. Gloria del Rocío Arbeláez Rodríguez, PhD. Coordinadora General de Investigación HECAM.
Dr. Roberto Carlos Ponce Pérez. Coordinador General de Control de Calidad HECAM.
Dra. Ximena Patricia Garzón Villalba, PhD. Coordinadora General de Docencia HECAM.
Dr. Roberto Vinicio Beletanga Carrión. Coordinador General de Hospitalización y Ambulatorio
HECAM.
Dra. Anabel Giovana Cifuentes Segarra. Presidenta del Comité de Ética Asistencial HECAM.
Dra. Marcela Elizabeth Zamora Matute. Jefa de Hematología HECAM.
Unidad Técnica de Hematología-HECAM.
Este protocolo médico de manejo clínico-terapéutico, provee de acciones basadas en
evidencia científica, con la finalidad de brindar atención oportuna y especializada en
beneficio del paciente.
Hematology Technical Unit HECAM.
This medical protocol of clinical-therapeutic management, provides actions based on
scientific evidence, in order to provide timely and specialized care for the benefit of the
patient.
Las enfermedades infecciosas emergentes y reemergentes son desafíos constantes para la salud pública en todo el mundo. Los casos recientes de neumonía de causa desconocida en Wuhan, China, han llevado al descubrimiento de un nuevo tipo de Coronavirus (2019-nCoV), que son virus de Ácido Ribonucleico (RNA) envueltos, de forma común encontrados en humanos, otros mamíferos y aves, capaces de causar enfermedades respiratorias, entéricas, hepáticas y neurológicas1.
La amenaza a la salud de la infección por Coronavirus 2 asociado al SRAS (SARS-CoV-2) y la enfermedad que produce el mismo llamada Enfermedad por Coronavirus (COVID-19) ya está establecida con sus tasas de infección y mortalidad de manera considerable más altas si se lo compara con otros virus respiratorios adquiridos en la comunidad2.
En tal sentido es necesario dar una respuesta por parte de la Unidad Técnica de Hematología en relación a esta pandemia con el ánimo de aportar al manejo integral de estos pacientes, homogeneizar criterios clínicos, lidiar de mejor manera con la incertidumbre en el diagnóstico y tratamiento de COVID-19.
El SARS CoV-2 y su enfermedad COVID-19, en la mayoría de pacientes tiene una presentación con síntomas leves. Sin embargo, en el 5% de los casos diagnosticados requerirán de una Unidad de Cuidados Intensivos (UCI)3, ya que presentan Síndrome de Dificultad Respiratoria Aguda (SDRA), shock séptico, Insuficiencia Multiorgánica y coagulopatía hemorrágica, así como trombótica, incluyendo Coagulación Intravascular Diseminada (CID), alcanzado en las salas de UCI una tasa mortalidad por COVID-19 entre el 22% al 62% en algunas series4. Adicional, se ha observado que el grupo de pacientes con mala evolución presentan un estado hiperinflamatorio, asemejándose al cuadro clínico descrito de una linfohistiocitosis hemofagocítica secundaria, que en este caso sería desencadenada por SARS CoV-25.
Un grupo de Hematólogos de diferentes hospitales de la ciudad de Quito: Especialidades Carlos Andrade Marín-Instituto Ecuatoriano de Seguridad Social (HECAM-IESS), Metropolitano; y, hospitales de la ciudad de Guayaquil: Teodoro Maldonado Carbo-IESS, Hospital Luis Vernaza y Clínica Gilbert, basados en la evidencia científica disponible y experticia profesional, elaboraron éste protocolo con las recomendaciones según los diferentes escenarios y complicaciones hematológicas.
Palabras clave: Infecciones por Coronavirus; Neumonía; Virus del SARS CoV2; COVID-19; tromboprofilaxis, anticoagulación, plasma convaleciente.
Emerging and reemerging infectious diseases are constant challenges to public health worldwide. Recent cases of pneumonia of unknown cause in Wuhan, China have led to the discovery of a new type of Coronavirus (2019-nCoV), which are enveloped ribonucleic acid (RNA) viruses, commonly found in humans, other mammals, and birds, capable of cause respiratory, enteric, liver and neurological diseases1.
The health threat of SARS-associated coronavirus 2 (SARS-CoV-2) and the disease that produces it called COVID-19 has already been established with its considerably higher infection and mortality rates compared to other respiratory viruses acquired in the community2.
In this sense, it is necessary to give a response from the Hematology Technical Unit in relation to this pandemic in order to contribute to the comprehensive management of these patients, homogenize clinical criteria, better deal with uncertainty in the diagnosis and treatment of COVID-19.
SARS CoV-2 and its disease COVID-19, in the majority of patients have a presentation with mild symptoms. However, in 5% of diagnosed cases they will require an Intensive Care Unit (ICU)3, since they present Acute Respiratory Distress Syndrome (ARDS), septic shock, Multiple Organ Failure and hemorrhagic coagulopathy, as well as thrombotic, including Coagulation Disseminated Intravascular (DIC), achieved in the ICU wards a mortality rate for COVID-19 between 22% and 62% in some series4. Additionally, it has been observed that the group of patients with poor evolution present a hyperinflammatory state, resembling the clinical picture of secondary hemophagocytic lymphohistiocytosis, which in this case would be triggered by SARS CoV-25.
The group of Hematologists from the hospitals of the city of Quito: Specialties Carlos Andrade Marín HECAM-IESS, Metropolitano; and, hospitals in the city of Guayaquil: Teodoro Maldonado Carbo-IESS, Luis Vernaza Hospital and Gilbert Clinic, based on the available scientific evidence and professional expertise, prepared this protocol with the recommendations according to the different hematological scenarios and complications.
Keywords: oronavirus infections; Pneumonia; SARS CoV2 virus; COVID-19; thromboprophylaxis; anticoagulation; convalescent plasma.
Dar una respuesta desde el punto de vista hematológico y articular la misma con los protocolos de manejo institucional y de las principales especialidades como: Emergencia, Cuidados Intensivos, Medicina Interna y Banco de Sangre del Hospital de Especialidades Carlos Andrade Marín.
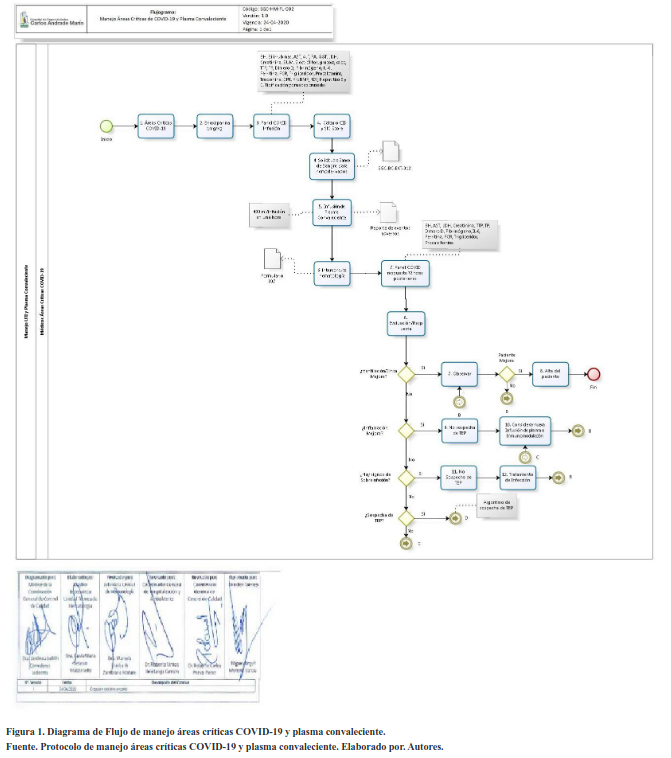
Este documento es un Protocolo clínico terapéutico, aplicado por los hematólogos, personal de Terapia Intensiva, Medicina Interna y Banco de Sangre como respuesta a diferentes escenarios y complicaciones hematológicas en COVID-19 a todos los pacientes COVID-19 [Clasificación internacional de enfermedades 10° edición (CIE-10): Coronavirus como causa de Enfermedades Clasificadas en otros Capítulos (B97.2)] del Hospital de Especialidades Carlos Andrade Marín.
En el paciente COVID-19 con desenlaces severos, existe una relación directa entre infección/inflamación/coagulopatía, por lo que tomando como base esto, se ha propuesto un acercamiento diagnóstico y terapéutico bajo 3 objetivos:
Las recomendaciones están dirigidas a pacientes con indicaciones de hospitalización y que se detallan a continuación en las actividades de este protocolo médico.
4.1 Prevención de trombosis y manejo de coagulopatía en
pacientes con COVID-19
Se asume que todos los pacientes enfermos con SARS COV 2 tienen un riesgo trombótico más elevado (Triada de Virchow), en especial los pacientes con enfermedad severa y aquellos ingresados en UCI.
Por esta razón, la aplicación activa de anticoagulación para algunos pacientes con COVID-19 severo ha sido recomendada por un consenso de expertos en China6 y se lo está utilizando por distintos centros en el mundo, a pesar de que su eficacia aún no ha sido validada.
Para la toma de decisiones a la hora de indicar dosis de fármacos anticoagulantes hemos decidido considerar como marcador al dímero D para los pacientes no ingresados en UCI y para los pacientes con estancia en UCI además de este marcador se realizará el cálculo de ̈Sepsis Induced Coagulopathy Score ̈ (SIC score)7.
4.1.1 Prevención de trombosis de pacientes con COVID-19
Recomendaciones generales al ingreso del paciente

4.1.2 Pacientes con alto riesgo de trombosis10
Recomendamos el inicio de enoxaparina a dosis intermedias, administrar HBPM subcutánea (SC) a 1 mg/Kg/día; si falla renal, Clearance de Creatinina (Clcr) < 30 ml/min, 40 mg (SC) cada día (QD).
4.1.3 Paciente ingresado a UCI
Recomendamos el inicio de enoxaparina a dosis intermedias, administrar HBPM (SC) a 1 mg/Kg/día; si falla renal, Clcr < 30 ml/min, 30 mg (SC-QD)
4.1.4 Indicación de anticoagulación.
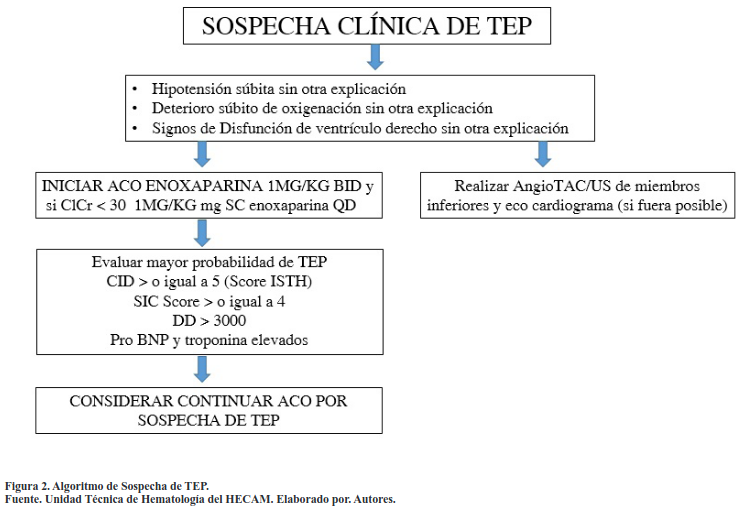
Deberá iniciar enoxaparina a dosis anticoagulantes (Tabla 3) a todo paciente con hipotensión y deterioro súbito de oxigenación y con signos de disfunción de ventrículo derecho sin otra explicación en el que se piensa sobreinfección o si el paciente tenía ya una sobreinfección previa, la procalcitonina esté disminuyendo o sea negativa.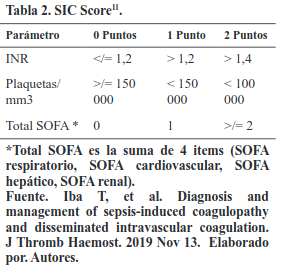

4.1.5 Pacientes al alta
**Valorar e individualizar indicación según persistencia de alto riesgo trombótico al alta.
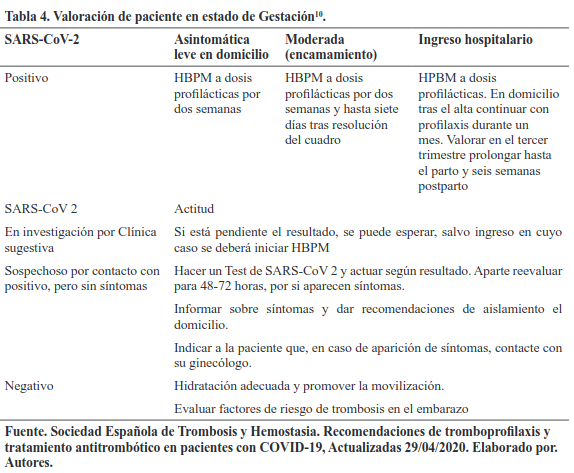
4.1.6 Pacientes embarazadas y puerperio10
Pacientes embarazadas son un grupo de riesgo aumentado de Enfermedad Tromboembólica Venosa (ETEV), si a esto se suma infección por COVID-19 deberá existir una valoración adecuada en el embarazo y en el puerperio.
4.2 Manejo del sangrado secundario a coagulopatía en pacientes con COVID-19.
Se debe recordar que los tiempos de coagulación alterados no ameritan corrección con soporte transfusional a menos que exista evidencia de sangrado activo14. El sangrado es raro en el contexto de COVID-19. Si se desarrolla un sangrado, se pueden seguir principios similares a la coagulopatía séptica según las pautas del ISTH en lo relacionado con respecto al apoyo con Plasmas Frescos Congelados (PFC) o crioprecipitados15.
4.2.1 Si se presenta sangrado mayor, transfusión terapéutica
***El soporte transfusional con PFC, crioprecipitados, plaquetas debe considerarse si existen las mismas alteraciones analíticas y serán sometidos a procedimientos invasivos.
4.2.2 Transfusión profiláctica (Pacientes sin sangrado)

Tang et al., en su estudio mencionan que el 71% de los pacientes críticos con COVID-19 que no sobrevivieron tenían CID utilizando la puntuación CID (ISTH), en comparación con sólo el 0,6% de sobrevivientes17.
Con lo anotado se podría generar recomendaciones para la identificación y tratamiento inmunomodulador con corticoides, IgG endovenosa, para un grupo de pacientes con COVID-19, portadores de hiperinflamación18 que se asocia con desenlaces severos (SDRA/terapia intensiva/muerte).
Propuesta de tratamiento de hiperinflamación secundario a SARS CoV-2 desde el punto de vista de Hematología.
Considerando que los resultados de ensayos clínicos controlados relacionados con inmunomodulación no estarán disponibles durante meses, y basado en las recomendaciones actuales de expertos, no hay justificación basada en la evidencia disponible y en la ética profesional para negar de formar categórica el uso de inmunomoduladores en una enfermedad con un franco estado inflamatorio y más aún frente a la posibilidad de presentarse en algunos casos una asociación con síndrome hemofagocítico secundario a SARS-CoV2.
6.1 Dosis Corticoides19,20
Si peso corporal <80 kg:
Si peso corporal ≥80 kg:
6.2 Dosis de Inmunoglobulina21
6.3 Indicación de Plasma Convaleciente
El plasma convaleciente y su efecto neutralizante del virus, en el contexto de una herramienta con mucha experiencia ganada a lo largo del tiempo en otras enfermedades emergentes; intervención que se encontraría cascada arriba del precepto infección / inflamación / SDRA / trombosis / muerte, lo convierten quizás en unas de las alternativas de mayor validez entre las escasas opciones terapéuticas que se dispone para COVID-1922.
El médico a cargo de la atención directa del paciente es quien llenará el formulario para la solicitud de plasma convaleciente al Banco de Sangre, en este sentido debe Interconsultar a la Unidad Técnica de Hematología para la indicación del mismo.
Se indicará en:
La administración del plasma deberá respetar la compatibilidad ABO, deberá ser de entre 200 y 400 ml de plasma y en caso de riesgo de sobrecarga se deberá poner la dosis más baja. La infusión intravenosa será lenta a un ritmo de 200 ml/h23,24.
Como en todas las transfusiones el personal de enfermería deberá mantener un registro de toma de signos vitales antes, durante y después de la transfusión y llenar el registro del Banco de Sangre y reportar los efectos adversos.
6.3.1 Recomendaciones para todos los pacientes previo a la infusión de plasma convaleciente
6.3.2 Seguimiento posterior a la infusión de plasma convaleciente
Es fundamental llevar un registro de los resultados obtenidos con los pacientes que reciban este tratamiento para su análisis y posterior toma de decisiones de tratamiento.
Se registrarán las siguientes características clínicas del paciente en las notas de los servicios de áreas críticas COVID 19 y Hematología:
Transcurridas 72 horas después de la infusión de plasma convaleciente se registrarán en la evolución de la Historia Clínica los siguientes resultados:
En el caso de sospecha de TEV/TEP.
Complicaciones y/o Desviaciones del protocolo
Puede existir desviación del protocolo debido a la individualización de tratamiento del paciente asociadas a complicaciones como parte de la evolución natural de la enfermedad.
Tromboprofilaxis y anticoagulación
Sangrados clínicamente relevantes, mayores y de sitio crítico (Clasificación de la ISTH).
Trombocitopenia asociada a heparina.
Plasma convaleciente
Reacciones transfusionales
Las reacciones transfusionales más comunes asociadas a la infusión de plasma son:
En caso de presentarse, se suspenderá el tratamiento y se aplicará un protocolo de manejo de reacciones transfusionales.
Dado que COVID-19 es una enfermedad emergente, no existe hasta el momento alternativas terapéuticas a las anotadas en este protocolo, cuya efectividad sea validada en ensayos clínicos controlados.
2019-n-Cov: Nuevo Coronavirus; RNA: Ácido Ribonucleico; SARS CoV2: Severe Acute Respiratory Syndrome coronavirus 2; COVID 19: Coronavirus Disease 19; UCI: Unidad de Cuidados Intensivos; SDRA: Síndrome de Dificultad Respiratoria del Adulto; CID: Coagulación Intravascular Diseminada; HECAM – IESS: Hospital Carlos Andrade Marín-Instituto Ecuatoriano de la Seguridad Social; CIE 10: Clasificación Internacional de Enfermedades 10° edición; B97.2: Coronavirus como causa de Enfermedades Clasificadas en otros Capítulos; UTI: Unidad de Terapia Intensiva; SIC: Sepsis Induced Coagulopathy; HBPM: Heparina de Bajo Peso Molecular; TP: Tiempo de Trombina; SC: Subcutáneo; ClCr: Clearance de Creatinina; QD: cada día; BID: dos veces al día; TID: tres veces al día; mg: miligramos; hg: kilogramos; TVP/TEP: Trombosis Venosa Profunda/Tromboembolia Pulmonar; INR: Ratio Internacional Normalizado; SOFA: Sequential Organ Failure Assessment; hrs: horas; mi. Mililitro; min: minuto; UI: Unidades Internacionales; IV: Intravenoso; aTTP: Tiempo Parcial de Tromboplastina activado; ETEV: Enfermedad Tromboembólica Venosa; PFC: Plasma Fresco Congelado; ISTH: International Society on Thrombosis and Haemostasis; SIC: Sepsis Induced Coagulopathy; C: grado Celsius; PCR: Proteína C Reactiva; TAC: Tomografía Axial Computarizada; AST: Aspartato Aminotransferasa; ALT: Alanina Aminotransferasa; FA: Fosfatasa Alcalina; GGT: Gamma Glutamil Transpeptidasa; LDH: Lactato Deshidrogenasa; BUN: Nitrógeno Ureico en sangre; TTP: Tiempo de Tromboplastina Parcial, TP: Tiempo de Protrombina; Interleucina-6; CPK: Creatina-fosfocinasa; TEP: Tromboembolia Pulmonar; mmol/L: milimoles por litro; IL-6: Interleuquina 6; NT-ProBNP: Fracción N-terminal del propéptido natriurético de tipo B; HIV: Virus de la Inmunodeficiencia Humana; BH: Biometría Hemática; PAFI: Índice de Presión/Fracción Inspirada de Oxígeno.
Todos los autores participaron en la concepción y diseño del trabajo, recolección y obtención de resultados, análisis e interpretación de datos, redacción del manuscrito, revisión crítica del manuscrito, aprobación de su versión final y asesoría técnica o administrativa.
Andrés Orquera Carranco. Médico, Universidad Central del Ecuador. Especialista en Hematología, Universidad San Francisco de Quito. Diploma Superior en Desarrollo Local y Salud, Universidad Técnica Particular de Loja. Diploma Superior en Educación en Ciencias de la Salud, Universidad Central del Ecuador. Médico Hematólogo, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quithttpso-Ecuador. ORCID: https://orcid.org/0000-0003-0143-2967.
Paola María Velasco Maldonado. Doctor en Medicina y Cirugía. Especialista en Medicina Interna, Universidad Católica de Santiago de Guayaquil. Medicina Especialista en Hematología, Universidad de Buenas Aires. Especialidad en Trasplante de Progenitores Hematopoyéticos, Sociedad Argentina de Hematología. Médica Especialista en Hematología, Coordinación General de Trasplantes, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador, ORCID: https://orcid.org/0000-0002-5915-9177.
Manuel Antonio Granja Morán. Médico, Universidad Central del Ecuador. Especialista en Hematología, Universidad San Francisco de Quito. Alta especialidad en Medicina Trasplante de Células Progenitoras Hematopoyéticas, Universidad Nacional Autónoma de México. Jefe (E) de la Unidad de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0002-9138-6353.
Mauricio Rodrigo Heredia Fuenmayor. Doctor en Medicina y Cirugía, Universidad Central del Ecuador. Especialista en Hematología, Universidad San Francisco de Quito. Diploma Superior en Medicina Transfusional, Universidad Central del Ecuador. Médico Tratante/A Especialista en Hematología 1, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-7607-9892.
María Fernanda Luján Jiménez. Doctora en Medicina y Cirugía, Pontificia Universidad Católica del Ecuador. Especialista en Hematología, Universidad San Francisco de Quito. Médico Tratante/A Especialista en Hematología 1, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-7292-7794.
Myriam Muñoz Guerra. Doctora en Medicina y Cirugía, Universidad Central del Ecuador. Especialista en Hematología, Universidad Técnica Particular de Loja. Diploma Superior en Medicina Transfusional, Universidad Central del Ecuador. Médica Hematóloga, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0002-2649-4008.
José Isidro Páez Espín. Doctor en Medicina y Cirugía, Universidad Central del Ecuador. Especialista en Hematología, Universidad Internacional del Ecuador. Médico Hematólogo, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-9471-1599.
Grace Paulina Salazar Vega. Médico, Universidad Central del Ecuador. Especialista en Hematología, Universidad San Francisco de Quito. Docente Hematología Pontificia Universidad Católica de Quito. Médico Tratante, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-6033-1280.
Erwing Bolívar Sánchez Paz. Doctor en Medicina y Cirugía, Universidad Central del Ecuador. Especialista Hematología, Universidad San Francisco de Quito. Médico Tratante, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0002-5938-6767.
Julia Edith Soria Silva. Doctor en Medicina y Cirugía, Universidad Central del Ecuador. Especialista en Hematología, Universidad Técnica Particular de Loja. Especialista en Gerencia de Salud, Universidad San Francisco de Quito. Médica Hematóloga, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-8484-0370.
Paulina del Rosario Vásconez Conrado. Doctor en Medicina y Cirugía, Universidad Central del Ecuador. Especialista en Hematología, Universidad Internacional del Ecuador. Especialista en Medicina Interna, Universidad Central del Ecuador. Diploma Superior en Medicina Transfusional, Universidad Central del Ecuador. Médica Hematóloga, Unidad Técnica de Hematología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID: https://orcid.org/0000-0001-5650-5268.
Se utilizaron recursos bibliográficos de uso libre y limitado. La información recolectada está disponible bajo requisición al autor principal.
El protocolo médico fue aprobado por pares y por las máximas autoridades.
La publicación fue aprobada por el Comité de Política Editorial de la Revista Médica Científica CAMbios del HECAM.
Se trabajó con recursos propios de los autores.
Los autores reportan no tener ningún conflicto de interés, personal, financiero, intelectual, económico y de interés corporativo.
A todo el personal de la Unidad Técnica de Hematología del Hospital de Especialidades Carlos Andrade Marín.