Abordaje endoscópico en el manejo de la fuga post manga gástrica.
Abordaje endoscópico en el manejo de la fuga post manga gástrica. |
Abordaje endoscópico en el manejo de la fuga post manga gástrica.
Endoscopic approach in the management of post gastric sleeve leakage.
Iván René Cantos Gavilanes1, Ronnal Patricio Vargas Córdova2
INTRODUCCIÓN. La fuga post manga gástrica es una complicación de los procedimientos bariátricos quirúrgicos, con prevalencia del 2,1%, en el que se emplea el abordaje endoscópico, describir su seguridad y éxito es relevante. OBJETIVO. Describir el abordaje endoscópico en el manejo de la fuga post manga gástrica. MATERIALES Y MÉTODOS. Revisión bibliográfica y análisis sistemático de artículos científicos. De un total de 384 artículos, 11 publicaciones de texto completo fueron seleccionados; 9 artículos fueron estudios retrospectivos y 2 revisiones sistemáticas. Los términos de búsqueda sobre el tratamiento endoscópico en fuga post manga gástrica se basaron en datos PubMed que cumplieron los criterios: leak, fístula, partial gastrectomy, gastrointestinal endoscopy. RESULTADOS. La literatura reportó seguridad con cero mortalidad y tasa de éxito para sutura endoscópica del 80,0%, over the scope clip 86,3%, drenaje interno endoscópico 83,41%, septotomía endoscópica 100,0%, stents endoscópicos hasta del 95,0% y terapia vacuum endoscópica 87,5%. CONCLUSIÓN. Se evidenció que el abordaje endoscópico en el manejo de la fuga post manga gástrica fue seguro y exitoso; se necesita personal experto en las diferentes modalidades terapéuticas reportadas.
Palabras clave: Obesidad; Gastrectomía; Fuga Anastomótica; Fístula; Endoscopía Gastrointestinal; Cirugía Bariátrica.
INTRODUCTION. Post gastric sleeve leakage is a complication of surgical bariatric procedures, with a prevalence of 2,1%, in which the endoscopic approach is used, describing its safety and success is relevant. OBJECTIVE. To describe the endoscopic approach in the management of post gastric sleeve leak. MATERIALS AND METHODS. Bibliographic review and systematic analysis of scientific articles. From a total of 384 articles, 11 full-text publications were selected; 9 articles were retrospective studies and 2 systematic reviews. Search terms on endoscopic treatment in postgastric sleeve leak were based on PubMed data that met the criteria: leak, fistula, partial gastrectomy, gastrointestinal endoscopy. RESULTS. The literature reported safety with zero mortality and success rate for endoscopic suture 80,0%, over the scope clip 86,3%, endoscopic internal drainage 83,41%, endoscopic septotomy 100,0%, endoscopic stents up to 95,0% and endoscopic vacuum therapy 87,5%. CONCLUSION. It was evidenced that the endoscopic approach in the management of post gastric sleeve leak was safe and successful; expert personnel are needed in the different therapeutic modalities reported.
Keywords: Obesity; Gastrectomy; Anastomotic Leak; Fístula; Endoscopy, Gastrointestinal; Bariatric Surgery.
El sobrepeso y la obesidad se han incrementado de manera exponencial en las últimas décadas, alcanzó al 61,1% de la población norteamericana, 58,4% en Europa y 56,0% en la región mediterránea oriental1, al igual que la prevalencia de la obesidad severa en México y Estados Unidos. Los procedimientos metabólicos y bariátricos han sido un tratamiento efectivo para el control de esta enfermedad2. Ng M, et al., describieron una prevalencia de obesidad en adultos a nivel mundial de 28,8% en 1980 a 36,9% en el 2013 en hombres y del 29,8% al 38,0% en mujeres3.
En Ecuador Pérez-Galarza, et al., estimaron una prevalencia de sobrepeso, obesidad y síndrome metabólico (SM) del 39,5%; 22,3% y del 31,2%, de forma respectiva; la obesidad abdominal fue mayor en hombres que en mujeres. El sobrepeso, la obesidad y el SM fueron más prevalentes en mujeres (65,7%), áreas urbanas (33,7%), áreas de baja altitud (0-500 metros sobre el nivel del mar) y en la clase económica alta (Quintil 4 y 5)4.
De acuerdo a la encuesta realizada por la Federación Internacional de Cirugía de la Obesidad y Trastornos Metabólicos (IFSO) en el 2018; de un total de 696 191 procedimientos quirúrgicos, la gastrectomía vertical en manga (GVM) fue el procedimiento quirúrgico metabólico/ bariátrico más realizado a nivel mundial en el 55,4%, seguido del bypass gástrico en Y de Roux con el 29,3%5. La GVM se realizó por primera vez en 1988 por Hess, es un procedimiento restrictivo que consiste en el grapado del extremo final de los vasos de la curvatura mayor; presenta baja tasa de complicaciones, menor tiempo operatorio, ausencia de anastomosis y de mal absorción; así como la preferencia del paciente y la factibilidad de conversión a otros procedimientos bariátricos6,7. Este procedimiento no está exento de complicaciones; Gagner, et al., reportaron 191 fugas de 8 920 gastrectomías verticales en manga, con una incidencia del 2,1% (0,5% al 7%)8,9, por su parte, Weiner, et al., registraron sangrado en el 2,7% (19; 686), hernia en el lugar del trocar, tromboembolismo venoso o embolia pulmonar en el 0,14% (1; 686), estenosis 0,8% (5; 686), reflujo gastroesofágico y deficiencia nutricional10.
La fisiopatología de la fuga de la línea de grapado no es clara pero se asocia a una hiperpresión intraluminal y a cambios en el aporte sanguíneo en la unión gastroesofágica7. Es una de las complicaciones más devastadoras, que en su mayoría resulta en sepsis abdominal, reintervenciones y muerte; además, pueden manifestarse como un absceso subfrénico cuya evolución podría conllevar a la formación de un absceso pulmonar y/o fístula gastro bronquial1. El objetivo del trabajo fue describir el abordaje endoscópico en el manejo de la fuga post manga gástrica.
Se realizó una revisión bibliográfica y un análisis sistemático de 384 artículos científicos que incluyeron el tratamiento endoscópico en fuga post manga gástrica encontrada en las bases de datos PubMed. Los artículos fueron: estudios en idioma inglés que cumplieron el criterio de búsqueda DECS “leak AND sleeve gastrectomy”; se filtró los datos obtenidos mediante los parámetros:“- full text”, “humans”, “english”, desde el año 2015 hasta diciembre 2020; se obtuvieron 391 resultados. En la búsqueda de literatura se incluyó todo tipo de documentos aportados por las sociedades y asociaciones profesionales que estudiaron el tratamiento quirúrgico de la obesidad y el abordaje de las complicaciones, se tomaron en consideración revisiones sistemáticas relevantes al estudio, se incluyeron 11 publicaciones: estudios originales retrospectivos 9 y revisiones sistemáticas 2, sobre el empleo de los diferentes abordajes endoscópicos en la fuga post manga gástrica empleando over the scope clip (OTSC) o drenaje endoscópico con doble pigtail. Se excluyeron 369 artículos que no registraron información sobre manejo endoscópico de fugas post manga gástrica, 2 por ser reportes de caso con un participante y 2 por ser comentarios.
Para el análisis se extrajo información de las variables: Grado de recomendación C, tasa de éxito, tiempo de curación de la fuga y morbilidad. De las revisiones sistemáticas se extrajo la efectividad del método endoscópico empleado para el manejo de la fuga gástrica, para apoyar los resultados, discusión así como las conclusiones y recomendaciones del estudio.
La revisión de la evidencia científica determinó: (Tabla 1)
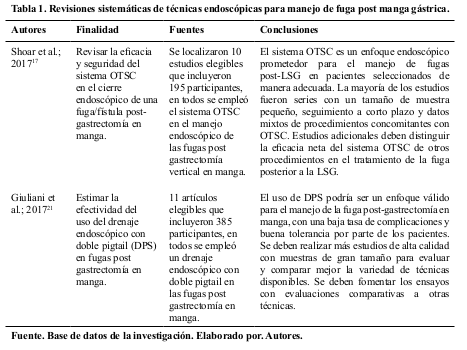
Se empleó un artículo sobre sutura endoscópica que reportó éxito en un 80,0% (4; 5), 2 artículos para el empleo de OTSC con éxito del 86,3%, 2 estudios para drenaje interno endoscópico 83,41%, 2 artículos para septostomía endoscópica 100,0%, 3 artículos para stents endoscópicos 95,0% y 1 artículo para terapia vacuum endoscópica con éxito del 87,5%. Tabla 2.
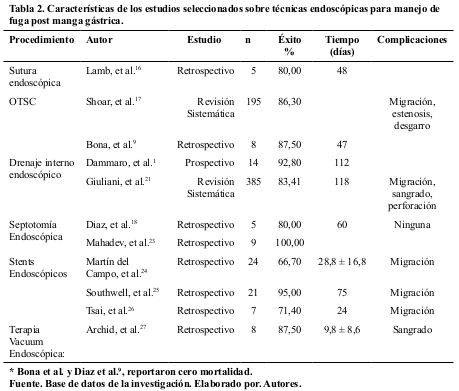
Una fuga se define como la extravasación del contenido intestinal debido a la disrupción de la línea de grapado o sutura con la subsecuente formación de colecciones intraabdominales11. Alizadeh, et al., reportaron una tasa de fuga del 0,7% de un total de 133 478 pacientes y evidenciaron factores asociados con riesgo incrementado de fuga tales como: dependencia de oxígeno, hipoalbuminemia, apnea del sueño, hipertensión arterial, diabetes, empleo de pruebas de provocación intraoperatorias y uso de drenaje12. Su presentación clínica fue con o sin estabilidad hemodinámica y/o sepsis abdominal9. Los signos tempranos de una fuga gástrica son: taquicardia, agitación, taquipnea y fiebre; de estos, la frecuencia cardiaca es el único parámetro fiable para diagnosticar en pacientes obesos (taquicardia 72-92%)10,13. En relación al tiempo de presentación, de acuerdo a la clasificación de Rosenthal, et al. se dividió en agudas (dentro de 7 días), tempranas (1-6 semanas), tardías (mayor a 6 semanas) y crónicas (mayor a 12 semanas), adicional se menciona una fuga persistente definida como una fuga residual diagnosticada al menos 7 días posteriores a una sutura laparoscópica no exitosa y drenaje peri visceral, siendo la localización más frecuente a nivel proximal en el 90,0%9,11. En el contexto de un paciente estable, el manejo conservador es una alternativa excelente en lugar de la cirugía que incluye el drenaje guiado por imagen de la colección infectada, antibióticos endovenosos, alimentación naso yeyunal e inserción de stents; si por el contrario, tenemos un paciente con signos y síntomas de sepsis abdominal, la re laparoscopía es la elección10. Los algoritmos se basan en el tiempo de presentación de la fuga, la presentación clínica y el estado nutricional14.
Se reportan diferentes modalidades terapéuticas mediante abordaje endoscópico entre ellas el empleo de stents metálicos recubiertos15, OTSC9, sutura endoscópica ya sea como tratamiento primario o terapia complementaria16, drenaje endoscópico con doble pigtail17 y la septotomía endoscópica en fugas crónicas con una tasa de éxito del 80,0%18. Figura 1.
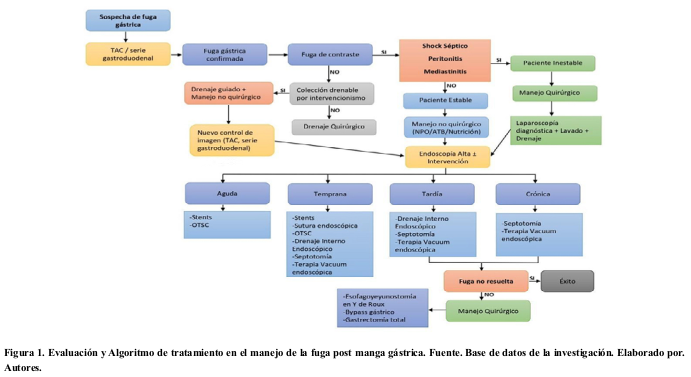
En una revisión sistemática realizada por Hughes, et al., en el 2019 con un total de 74 pacientes descritos en 20 artículos reportaron una tasa de éxito del 76,0% al emplear el manejo quirúrgico como terapia de primera línea con un abordaje laparoscópico inicial cuyos procedimientos realizados fueron: lavado peritoneal, colocación de drenaje y reforzamiento de la línea de grapado; sin embargo, 22,0% necesitó usar como segunda línea al abordaje endoscópico, siendo la colocación de stents el más común a emplearse y en todos los artículos reportaron una mortalidad del 9,7% con el manejo quirúrgico como primera línea19. Nguyen, et al., argumentaron sobre lo controversial del tratamiento quirúrgico en primera instancia debido al proceso inflamatorio local y a una inadecuada perfusión tisular, recalcaron su relación de acuerdo al estado del paciente; sin embargo, reportaron una alta morbilidad de hasta el 50,0% con una mortalidad del 2–10%; 48,0% de tasa de conversión a cirugía abierta, y se recomendó la opción quirúrgica a las 12 semanas posteriores al manejo conservador fallido, siendo la esofagoyeyunostomía en Y de Roux una técnica efectiva y segura, puede también realizarse bypass gástrico o gastrectomía total13. La cirugía debería ser utilizada en el manejo de fugas crónicas post GVM, Nedelcu, et al., indicaron que la cirugía debe ser considerada cuando haya fallado en primera instancia el abordaje endoscópico, además de reportar de la presencia de fugas en los procedimientos quirúrgicos definitivos tales como bypass gástrico en Y de Roux, fistuloyeyunostomía y anastomosis esofagoyeyunal (37,5%, 21,9% y 7,7%, respectivamente) 20. Dentro del manejo conservador mediante terapia antibacteriana y suplemento nutricional, Hughes, et al., reportaron una tasa de éxito del 82,0% como terapia de primera línea, el cual podía emplearse en conjunto con drenaje percutáneo de colecciones intraabdominales19. Bashah, et al., describieron un algoritmo de manejo conservador y reportaron de un total de 73 pacientes con fuga post manga gástrica, una tasa de éxito en el manejo conservador del 97,1%, todos presentaron resolución en 8,8 ± 0,72 semanas; se reportan también complicaciones como re fuga en el 14,9% y absceso esplénico en el 2,9%. Adicional, reportaron tener resolución más temprana de la fuga en aquellos pacientes con alimentación yeyunal14. Existen diversas técnicas endoscópicas en la literatura actual que pueden ser empleadas en el abordaje terapéutico de las fugas post gastrectomía vertical en manga: Sutura endoscópica, que se emplea para el cierre de la fuga gástrica, aunque la evidencia es limitada referente a su uso en fugas y fístulas en GVM y bypass gástrico. En los pacientes tratados exitosamente con esta técnica, se permite un pronto inicio de la alimentación por vía oral; así como la interrupción de la contaminación intra abdominal. Lamb, et al., describieron el uso de esta técnica en un muestra muy pequeña de 5 pacientes y el éxito en 4 de ellos en un tiempo promedio de 48 días, recalcaron además la necesidad de experiencia considerable para realizar esta técnica16; OTSC, que consiste en el cierre del defecto mediante la colocación de clips, aproximando sus bordes y permitiendo así su cicatrización. Shoar, et al., en su revisión sistemática incluyeron a 195 pacientes con fuga/fístula post GVM, siendo la localización proximal más común, seguido de la parte media y la parte distal (84,5%, 5,9% y 4,7%, respectivamente). De esta población solo 73 fueron tratados con el sistema OTSC y reportaron una tasa de éxito del 86,3% en el cierre de la fuga gástrica. Adicional, el 63,5% necesitó un solo clip. Las complicaciones reportadas en relación al OTSC son migración, estenosis y desgarro en el 1,8%, y describieron la evidencia de fuga gástrica persistente en el 9,3%21. Bona, et al., describieron una estrategia que consiste en la combinación del OTSC y un stent por 5 a 6 semanas, con un total de 8 pacientes reportó una tasa de curación del 87,5% en un tiempo promedio de 47 días, morbilidad del 25,0% y sin mortalidad asociada al procedimiento; además se reportó una complicación en relación a sangrado de la mucosa autolimitado9; Drenaje interno endoscópico (DIE), que se basa en la colocación de stents a nivel de la fuga, permitiendo el drenaje del absceso hacia la cavidad gástrica, lo que a su vez permite el control local con posterior cierre de la fuga gástrica. Dammaro, et al., señalaron que los pacientes estables con fuga gástrica fueron tratados sólo con drenaje interno endoscópico, sonda de alimentación nasoyeyunal y antibióticos, y recalcó la importancia de crear protocolos que eviten la cronicidad de las fugas post GVM. A su vez, en pacientes hemodinámicamente inestables la elección fue mediante relaparoscopía y drenaje externo1. Se estudió a 14 pacientes en quienes como primer paso se realizó relaparoscopía + drenaje externo y posterior a 4 días realizaron el drenaje interno endoscópico con doble stent pigtail (7-10 Fr), luego de 2 días empiezan la movilización del drenaje externo (2 cm por día) independientemente del volumen de producción, hasta que desciende su producción y es retirado. Además de realizar controles endoscópicos cada 4 semanas hasta el cierre de la fuga1. Un intervalo de tiempo de 112 días fue necesario para la resolución. El 78,6% de los pacientes tuvieron una curación temprana con la remoción del DIE en el primer control endoscópico. El empleo del DIE tiene una tasa de curación del 92,8%, el protocolo mencionado falló la resolución en un paciente (7,2%) por retraso en el manejo endoscópico que degeneró en una gastrectomía total como tratamiento definitivo1. En una revisión sistemática del 2019 de Giuliani, et al., con 385 pacientes, de los cuales se reportaron el cierre global de la fuga en un 83,41% utilizando DIE con doble stent, se mencionó que puede ser empleado como terapia de primera y segunda línea con un éxito del 84,71% y 78,05%, de forma respectiva. El tiempo promedio hasta la curación fue de 118,1 días y 13,73% de complicaciones (sangrado, migración del drenaje, perforación, fístula gastro bronquial, úlcera, peritonitis, entre otras), siendo a su vez más frecuente (47,0%) si se usa como terapia de segunda línea (4,7% como primera línea)17. Septostomía Endoscópica, que consiste en dividir el septo que separa el lumen gástrico de la cavidad del absceso, permitiendo el drenaje de la colección al equilibrar la presión tanto a nivel gástrico como del absceso; sin embargo, solo puede ser realizada cuando se tiene una cavidad del absceso bien definida sin comunicación con la cavidad abdominal18,22. Se ha descrito el uso de esta técnica en fugas tempranas y crónicas. Diaz, et al., en un estudio retrospectivo de 5 pacientes en quienes los tratamientos previos fueron fallidos (limpieza quirúrgica, drenajes, stents u OTSC), realizaron septostomía endoscópica. El tiempo promedio al diagnóstico fue de 15 días, 100,0% de las fugas se evidenciaron en el tercio superior, el tiempo promedio al momento de realizar la septostomía fue de 61 días y el tiempo promedio de resolución fue de 60. No reportó morbilidad o mortalidad asociada al procedimiento con una tasa de éxito del 80,0%18. Mahadev, et al., han sugerido que esta técnica puede ser segura y efectiva incluso en pacientes refractarios a otros abordajes endoscópicos, se requiere en promedio 2,3 septostomía hasta su curación evidenciada en los 9 pacientes de su estudio, en 3 de ellos perduró la comunicación del lumen gástrico y la cavidad peri gástrica, y ninguno necesitó cirugía de revisión23; Stents endoscópicos, que pueden ser no recubiertos o recubiertos parcial o totalmente, deben colocarse entre 3–5 cm proximales a la línea z y 5 cm distal a la fuga. Martín del Campo, et al., describieron un estudio en el cual emplearon stents autoexpandibles recubiertos en su totalidad en conjunto con pegamento de fibrina, con un total de 24 pacientes, de estos el 79,2% (19 pacientes) presentaron la fuga a nivel proximal. El tiempo promedio de permanencia del stent fue de 28,8 ± 16,8 días y en el 20,8% se realizó el retiro temprano del stent debido a vómito incoercible con o sin reflujo24. En el 41,7% se necesitó adicionar o reemplazar el stent (1-4 stents) para lograr la curación de la fuga, en el 16,7% no fue necesario otro procedimiento. Se reportó migración del 22,0% de los stents. El uso de procedimientos suplementarios fue necesario con pegamento de fibrina, sutura endoscópica, clips endoscópicos, septostomía endoscópica, dilatación con balón o la aplicación de agentes esclerosantes. Tres pacientes se perdieron durante el seguimiento, de los 21 pacientes restantes. El 66,7% tuvo resolución de la fuga en un tiempo promedio de 61,5 días (100,0% de curación en fugas agudas) y en el 23,8% se presentó fuga persistente que necesitó cirugía de revisión24. En cambio, Southwell, et al., de un total de 21 pacientes, con empleo de stents metálicos autoexpandibles en conjunto con procedimientos suplementarios, reportaron una tasa de resolución del 95,0% en un tiempo promedio de 75 días y con 5 intervenciones endoscópicas. Además, de una tasa similar de migración del 19,0%25. Tsai, et al., describieron su uso en pacientes post GVM o en bypass duodeno yeyunal en asa con GVM, sin embargo, la muestra es de 7 pacientes, de los cuales 5 tuvieron un manejo exitoso con su uso temprano26; Terapia vacuum endoscópica (TVE), que consiste en colocar un sistema de drenaje de esponja intraluminal en el sitio de entrada al defecto, luego se aplica presión negativa que permite el drenaje del absceso y conlleva al cierre de la lesión. Archid, et al., reportaron 8 pacientes con el empleo de esta modalidad terapéutica, con un éxito del 87,5% (7 pacientes), con un tiempo de TVE de 9,8 ± 8,6 días, 3,3 ± 2,2 endoscopias y 19,0 ± 15,1 días de hospitalización27. Se reportó una complicación asociada a sangrado desde un vaso gástrico corto, el cual fue resuelto mediante embolización angiográfica. Se recomendó el inicio inmediato de TVE, inclusive durante la primera endoscopía, permitiendo el diagnóstico y tratamiento en una fase, sumado en ocasiones al control local de la infección mediante drenaje guiado por imagen o laparoscopía27.
Se evidenció que el abordaje endoscópico en el manejo de la fuga post manga gástrica fue seguro y exitoso; se necesita personal experto en las diferentes modalidades terapéuticas reportadas.
SM: Síndrome metabólico, IFSO: International Federation for the Surgery of Obesity and Metabolic Disorders, GVM: Gastrectomía vertical en manga, OTSC: Over the scope clip, DIE: Drenaje interno endoscópico, TVE: Terapia vacuum endoscópica.
IC: Recolección de información. IC, RV: Concepción y diseño del trabajo, Análisis e interpretación de datos, Redacción del manuscrito, Revisión crítica del manuscrito, Aprobación de su versión final y Rendición de cuentas.
Iván René Cantos Gavilanes. Médico, Especialista en Cirugía General, Universidad Central del Ecuador. Médico Especialista en Cirugía General, Cirugía General, Hospital General del Norte de Guayaquil los Ceibos. Guayaquil-Ecuador. ORCID: https://orcid.org/0000-0002-3664-5850
Ronnal Patricio Vargas Córdova. Doctor en Medicina y Cirugía, Especialista en Cirugía General, Universidad Central del Ecuador. Diploma Superior en Desarrollo Local y Salud, Especialista en Gerencia y Planificación Estratégica en Salud, Magister en Gerencia de Salud para el Desarrollo Local, Universidad Técnica Particular de Loja. Alta Especialidad en Medicina Cirugía Bariátrica, Universidad Nacional Autónoma de México. Líder, Clínica de Obesidad, Hospital General San Francisco IESS. Jefe, Departamento de Investigación y Docencia, Hospital General San Francisco. Quito–Ecuador. ORCID: https://orcid.org/0000-0001-5487-4000
Se utilizaron recursos bibliográficos de uso libre y limitado. La información recolectada está disponible bajo requisición al autor principal.
La publicación fue aprobada por el Comité de Política Editorial de la Revista Médica Científica CAMbios del HECAM en Acta 002 de fecha 20 de mayo de 2021.
Se trabajó con recursos propios de los autores.
Los autores reportaron no tener ningún conflicto de interés personal, financiero, intelectual, económico y de interés corporativo.
Agradecemos al Dr. Oscar Flores, por su soporte y apoyo metodológico para la elaboración de este trabajo; así como a colegas y amigos del departamento de docencia e investigación del Hospital General San Francisco.