Aplicación de la escala de MELD en los pacientes del Programa de Trasplante Hepático
Aplicación de la escala de MELD en los pacientes del Programa de Trasplante Hepático |
Aplicación de la escala de MELD en los pacientes del Programa de Trasplante Hepático
Application of the MELD scale in patients of the Liver Transplant Program
Ximena Alexandra Armijos Salinas1, John Byron Abad González2, Nancy Jhoana Rivera Armijos3, Stefanny Ibeth Viteri Ávila2, María José Fiallos Reinoso2, Jefferson Santiago Piedra Andrade4.
INTRODUCCIÓN. La escala Model for End-Stage Liver Desease se utiliza para conocer el estadio de la enfermedad hepática y para la asignación de órganos en los pacientes candidatos a trasplante. OBJETIVO. Validar la utilidad de la escala en pacientes adultos del Programa de Trasplante Hepático y su aplicación en la priorización de injertos para pacientes en lista de espera. MATERIALES Y MÉTODOS. Estudio observacional, descriptivo. De una población de 103 Historias Clínicas, se tomó una muestra de 95 registros del Programa de Trasplante Hepático del Hospital de Especialidades Carlos Andrade Marín en el período mayo 2016 a marzo 2020. Criterios de inclusión: datos de pacientes con diagnóstico de enfermedad hepática terminal, de ambos sexos, con edades comprendidas entre 14 y 65 años. La información se tomó del sistema AS400 y se analizaron en el programa estadístico International Business Machines Statistical Package for the Social Sciences, versión 23.0 y el estimador Kaplan-Meier. RESULTADOS. La sobrevida en lista de espera fue del 86,3% (82; 95) y en el post trasplante del 72,5% (44; 62) a los 12 meses y 68,9% (42; 62) a los 46 meses de seguimiento. DISCUSIÓN. Esta escala se consideró para los pacientes graves, asignándoles un puntaje que les permitió tener la opción de recibir un trasplante en relación a otros pacientes. CONCLUSIÓN. Se validó la utilidad de la escala, no se encontró diferencia significativa, pero mantuvo el principio de prioridad para los pacientes con mayor severidad.
Palabras clave:Cirrosis Hepática; Encefalopatías; Pronóstico; Registros Médicos; Sobrevida; Trasplante de Hígado.
INTRODUCTION. The Model for End-Stage Liver Desease scale is used to determine the stage of liver disease and for organ allocation in transplant candidates. OBJECTIVE. To validate the usefulness of the scale in adult patients of the Liver Transplantation Program and its application in the prioritization of grafts for patients on the waiting list. MATERIALS AND METHODS. Observational, descriptive study. From a population of 103 Medical Records, a sample of 95 records was taken from the Liver Transplantation Program of the Carlos Andrade Marín Specialty Hospital in the period may 2016 to march 2020. Inclusion criteria: data from patients with a diagnosis of terminal liver disease, of both sexes, aged between 14 and 65 years. The information was taken from the AS400 system and analyzed using the International Business Machines Statistical Package for the Social Sciences, version 23.0 and the Kaplan-Meier estimator. RESULTS. Survival on the waiting list was 86,3% (82; 95) and post-transplant survival was 72,5% (44; 62) at 12 months and 68,9% (42; 62) at 46 months of follow up. DISCUSSION. This scale was considered for seriously ill patients, assigning them a score that allowed them to have the option of receiving a transplant in relation to other patients. CONCLUSIONS. The utility of the scale was validated, no significant difference was found, but it maintained the principle of priority for patients with greater severity.
Keywords:Liver Cirrhosis; Brain Diseases; Prognosis; Medical Records; Survival; Liver Transplantation.
En 1963 en la ciudad de Denver de los Estados Unidos por Tomas Starzl se realizó el primer Trasplante Hepático (TH) en un paciente pediátrico, con los posteriores avances relacionados a: técnicas quirúrgicas, anestesia, utilización de drogas inmunosupresoras, mejoras en el manejo post trasplante en salas de terapia intensiva, lo que permitió tener mejores resultados en cuanto a la sobrevida de pacientes que está alrededor del 90% en el primer año post trasplante1.
Para estudiar a los pacientes candidatos a TH se usaron herramientas que permitieron conocer el estado de la enfermedad hepática, como la escala de Child-Pugh, que ingresaba en lista de espera a los pacientes que tenían la posibilidad de sobrevida global mayor al 90% al año post trasplante, correspondió a los pacientes con Child 7B, que no tuvieran complicaciones que afecten los resultados como peritonitis bacteriana espontánea o sangrado digestivo, además, el uso de esta escala en relación a la asignación y distribución de órganos de donantes fallecidos no se vio un impacto importante2.
Después en el 2002 se utilizó el Model for End-Stage Liver Disease (MELD) como índice pronóstico predictivo, basado en 3 variables analíticas simples: la bilirrubina, la creatinina sérica y el Cociente Internacional Normalizado (INR) del tiempo de protrombina, la utilidad de esta herramienta para la asignación de órganos priorizó a los enfermos graves, lo que disminuyó la mortalidad de los pacientes en lista de espera3.
El MELD surgió como un modelo para predecir la supervivencia en pacientes sometidos a la colocación de un Transyugular Porto Sistemic Shunt (TIPS) o shunt porto sistémicos desarrollado en la Clínica Mayo. Por los buenos resultados predictivos obtenidos se empezó a utilizar en los pacientes cirróticos candidatos a trasplante4 y dentro de las políticas de priorización se demostró que este sistema logró: limitar la inclusión inadecuada de pacientes y disminuir el tiempo de espera sin una excesiva repercusión en los resultados del trasplante, a pesar de la mayor gravedad. Esta escala no se ha utilizado en ciertas patologías que puedan ser tratadas con el trasplante, así por ejemplo: el Hepatocarcinoma (HCC), pacientes con cirrosis que tienen score bajo y presentan complicaciones como: ascitis refractaria, encefalopatías, síndrome hepatopulmonar, hiperoxaluria primaria y el prurito intratable. Esta situación otorgó la asignación de puntos extras para que alcancen un valor superior5.
Al momento que se empezó a utilizar esta escala se comparó con la escala de Albumina/ Bilirrubina (ALBI) para calcular la mortalidad en pacientes con cirrosis más HCC, sin embargo, no demostró ser mejor que la escala de MILAN6. Esta herramienta se utilizó para conocer la indicación de trasplante en los pacientes con HCC del programa de TH.
Se creó varios modelos de escala como: Cronic Liver Failure (CLIF) y el MELD modificado al agregar el valor del sodio, ya que los pacientes con hiponatremia [<135 miliequivalente/litro (meq/l)] demostraron mayor gravedad. Estas herramientas fueron importantes en cada etapa de la enfermedad hepática, para la priorización y asignación de donantes7.
El MELD tiene ventajas sobre otras escalas porque evita las valoraciones subjetivas de la presencia de ascitis o grado de encefalopatía, que se obtiene al usar métodos prospectivos, fiables y no tiene los defectos estadísticos que presenta el modelo de Pugh-Child. Esta escala parece ser útil como modelo pronóstico de supervivencia en pacientes con enfermedad hepática crónica en diversas circunstancias. En los EE.UU. se demostró que el MELD tiene un alto grado de concordancia para predecir mortalidad en lista de espera en una amplia cohorte de candidatos a trasplante hepático8,9. Por su objetividad y facilidad de aplicación, tiene una mejor utilidad para conocer el pronóstico de sobrevida global en el post trasplante, es decir, que mientras mayor es el valor, la mortalidad aumenta, así como también el riesgo de presentar complicaciones postquirúrgicas que a su vez prologan el tiempo de estancia hospitalaria. Para conocer esta predicción Freeman R, et al., comparó los resultados antes y después desde que se implementó su uso, uno de los beneficios fue una mejor disponibilidad del número de donantes de hígado, la asignación a los pacientes graves (prioridad al de mayor puntaje), lo que sirvió para mejorar los resultados de mortalidad en lista de espera, y otorgó la oportunidad de trasplante a los de mayor gravedad9. También, se pudo evitar que los pacientes compensados con bajo score ingresen al programa. En algunos trabajos la mortalidad en la lista de espera se redujo hasta en el 3,5% y no tuvo mayor impacto en la sobrevida del post trasplante a excepción de los que tuvieron puntaje mayor a 24 considerados demasiado graves10.
La modificación del MELD clásico al incorporar el sodio ha servido para mejorar la prioridad y la asignación a pacientes graves, porque puede aumentar el valor hasta en 3 a 5 veces del score, pero no está claro para determinar el pronóstico de sobrevida en el post trasplante. En algunos lugares podría utilizarse incluso como factor para definir el beneficio real del trasplante en pacientes que según el valor del MELD sodio supere los 40 puntos, lo que otorga la interpretación de paciente crítico y con posibilidades de no superar el procedimiento; esto aumenta la mortalidad peri operatoria11. Existió una dependencia significativa entre la hiponatremia y una mejor posición de la lista de espera12.
Texeira de Freitas A, et al., realizaron estudios del MELD en pacientes con puntaje suplementario por HCC (sobrevida a los 3 meses de 82,1% y 76,9%), se comparó con pacientes cirróticos sin tumor (3 meses 78,5% y 75,3% al año), esta fue poco subjetiva porque los pacientes con HCC en lista de espera fueron menos graves y para tener la opción de ser trasplantados requirieron la asignación de puntaje suplementario13.
El valor predictivo del MELD para el post operatorio inmediato en el día 5, 9 y 15, utilizado por Dashti H, et al., evidenciaron que los pacientes que no sobrevivieron al trasplante tuvieron mayor score14. Otros estudios científicos de su valor predictivo en los pacientes que se trasplantaron con donante vivo relacionado, donde no se encontró diferencia en los resultados obtenidos, pero existieron factores importantes que tuvieron impacto directo en el post trasplante inmediato, con la diferencia en la técnica quirúrgica del donante vivo adulto que es un procedimiento de mayor complejidad15.
En el Ecuador las enfermedades hepáticas terminales y crónicas están catalogadas dentro del grupo de catastróficas, por lo que los trasplantes son financiados por el gobierno. La actividad de TH inició en el 2009 en la ciudad de Quito, existen 5 centros acreditados con un número promedio entre 20 y 25 trasplantes por año16. En el Hospital de Especialidades Carlos Andrade Marín (HECAM) la escala Child-Pugh se usa en las valoraciones del estado de la enfermedad hepática antes del trasplante y utiliza criterios subjetivos clínicos como encefalopatía y ascitis, pero no supera a los resultados obtenidos por los parámetros del MELD que analiza valores de laboratorio y refleja la capacidad de síntesis de la función hepática17. El objetivo de este estudio fue validar la utilidad de la escala Model for End-Stage Liver Disease en pacientes adultos del Programa de Trasplante Hepático y su aplicación en la priorización de injertos para pacientes en lista de espera.
Estudio observacional, descriptivo, con una población de 103 datos de Historias Clínicas se tomó una muestra de 95 pacientes del Programa de Trasplante Hepático del Hospital de Especialidades Carlos Andrade Marín, en el período mayo 2016 a marzo 2020. Criterios de inclusión: pacientes con diagnóstico de enfermedad hepática terminal y pos trasplantados con seguimiento durante 46 meses, edad comprendida entre 14 y 65 años, con previa firma de Consentimiento Informado de Investigación, Compromiso de Confidencialidad de la Información y Autorización del Comité de Ética en Investigación en Seres Humanos (CEISH) HCAM. Se consideraron como criterios de exclusión: pacientes con falla hepática fulminante, tumores que no tenían posibilidad de valorar MELD, menores de 13 años de edad, pacientes en lista de espera que fueron inactivados de manera definitiva por diferentes aspectos y no se beneficiaron del trasplante.
La información se recolectó de la base de datos de las Historias Clínicas de cada paciente registrado en el sistema AS400 del HECAM. Para la tabulación y el análisis se aplicó el programa estadístico International Business Machines Statistical Package for the Social Sciences, (IBM SPSS) versión 23.0 y se utilizó el Estimador Kaplan-Meier.
De la muestra de 95 pacientes que ingresaron al programa, el 43,16% (41; 95) fueron mujeres y 56,8% (54; 95) hombres, con una edad media de 51,42% (±13,86). La media del Índice de Masa Corporal (IMC) de los pacientes fue 25,9% (±4,53).
Se determinaron los grupos sanguíneos de los pacientes que ingresaron a lista de espera, donde fue frecuente el grupo ORh+ con 73,68% (70; 95), seguido de ARh+ 12,63% (12; 95), BRh+ 9,47% (9;95), ORh- 3,16% (3; 95) y ABh+ 1,05% (1; 95).
El diagnóstico frecuente fue Cirrosis Hepática Criptogénica de acuerdo al diagnóstico de ingreso a la Lista de Espera Única Nacional (LEUN), como consta en el registro del Instituto Nacional de Donación y Trasplante de Órganos Tejidos y Células (INDOT). Tabla 1.
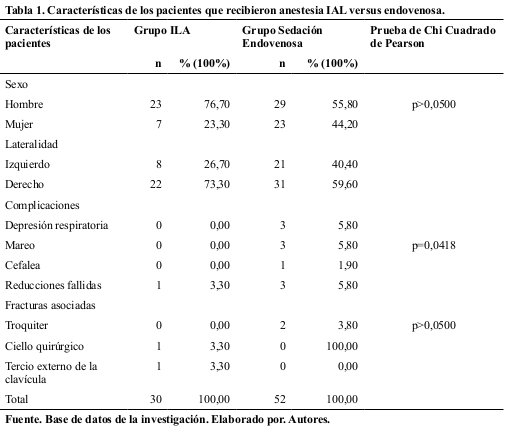
Según la clasificación del MELD se encontró que el mayor número de trasplantados fueron los grupo 3 y 4, pacientes con mayor gravedad. Tabla 2.

La media global del MELD de los pacientes en lista de espera fue 17,50(±5,09), y la media del tiempo en lista de espera hasta el punto de cohorte de la investigación fue 56,25(±87,90). Tabla 3.
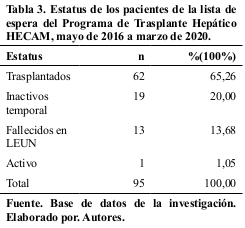
El total de trasplantes hepáticos realizados fue 65,26% (62; 95), el 34,73% (33; 95) restante correspondieron a los pacientes inactivos temporal, activo y fallecidos.
La sobrevida en lista de espera fue del 86,3% (82; 95), con 13,68% (13; 95) de pacientes fallecidos, mismo que se distribuyó por grupo según la tabla 4.

Los pacientes que han ingresado al programa de TH del HECAM fueron de las siguientes instituciones de salud: Ministerio de Salud Pública (MSP) 10,53% (10; 95), Instituto Ecuatoriano de Seguridad Social (IESS) 86,32% (82; 95) Instituto de Seguridad Social de las Fuerza Armadas (ISSFA) 3,16% (3; 95).
La supervivencia global del post trasplante fue de 72,5% a los 12 meses y del 69,4% a los 46 meses de forma respectiva. Figura 1.
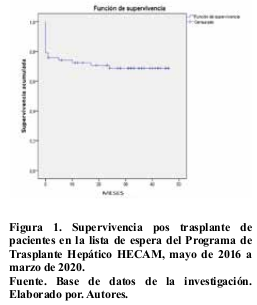
La supervivencia a los 12 meses de seguimiento en la escala MELD fue: grupo 1 (83,3%), grupo 2 (83,3%), grupo 3 (73,2%), grupo 4 (65%) con valores estadísticos no significativos (Log-Rank global p=0,394). Tabla 5 y Figura 2.

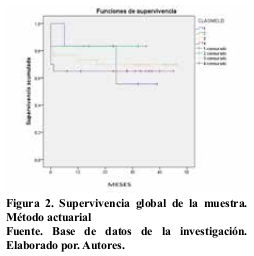
Para la validación de MELD y estimación del valor predictivo de esta escala, se implementó un análisis de curva ROC. Para el análisis de sobrevida se utilizaron el modelo actuarial, y el modelo de Kaplan-Meier, se verificó la significancia estadística a través del estadígrafo Log-Rank (p < 0,05).
En la comparación de las clasificaciones mediante el análisis de curvas de sobrevida se obtuvo un área bajo la curva de 0,59% para MELD. Figuras 3 y 4.
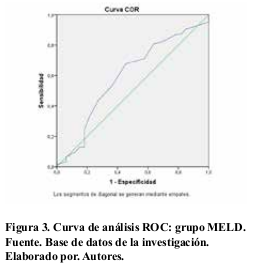
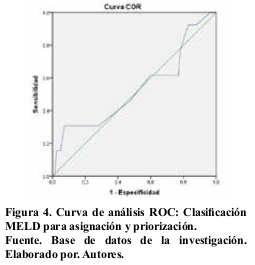
En este estudio se realizó una validación con el MELD para predecir la sobrevida de los pacientes que recibieron un TH con los que estuvieron en lista de espera. Al comparar la sobrevida mediante las curvas de Kaplan Meier en la escala de MELD, se observó que no existieron diferencias significativas entre los grupos de menor y mayor severidad. Este resultado nos permitió inferir que, el uso del sistema MELD para establecer el pronóstico no implicó una gran diferencia en el alistamiento para TH, y facilitó validarlo como un sistema fiable al contar con variables objetivas, para la inclusión en lista de espera de trasplante y asignación de órganos en el país.
Kartoun U, et al., hicieron modificaciones al MELD, al agregar variables como colesterol, edad, contaje de glóbulos blancos y otros, a este nuevo modelo de escala lo llamaron MELDS-Plus, para medir la mortalidad del paciente cirrótico a 90 días, se obtuvo resultados positivos con una mejora en la predicción entre un 8 y 10% comparándolo con el MELD-Sodio. En el Programa de TH en el HECAM no se encontró diferencias significativas por lo que se sugiere mejorar las escalas predictivas18.
Schlegel A, et al., compararon los resultados del MELD alto vs MELD bajo, con otros predictores de morbilidad en un grupo de pacientes trasplantados donde se observó que los pacientes que iban al trasplante con puntaje alto (mayor a 30) aumentó la mortalidad en un 12% y el 94% de pacientes presentaron alguna complicación, entre estas por ejemplo: mayor número de fugas biliares, mayor requerimiento de estancia hospitalaria por falla renal post quirúrgica, pero existió mayor afectación en la función del injerto. Esto se definió como se conoce, mayor MELD paciente de mayor gravedad19.
Jeroen Laurens Ad van Vugt et al., utilizó el grado de desnutrición de los pacientes por sarcopenia más el puntaje de MELD para calcular la mortalidad del paciente en lista de espera, donde observó que los pacientes con desnutrición marcada y MELD alto presentaron mayor riesgo de mortalidad en lista de espera20.
Esta investigación base servirá para ampliar futuras validaciones de la escala MELD en cada grupo etiológico de hepatopatía crónica.
Se validó la utilidad de la escala Model for End-stage Liver Disease y se observó que con un score mayor, la mortalidad aumenta, sin embargo, no se encontró diferencia significativa, pero se mantuvo el principio de prioridad en la asignación para los pacientes con mayor severidad.
TH: Trasplante Hepático; MELD: Model for End-stage Liver Disease; INR: Cociente Internacional Normalizado; CLIF: Cronic Liver Failure; mEq/l: miliequivalente/ litro HCC: Hepatocarcinoma; ALBI: Albumina/Bilirrubina; HECAM: Hospital de Especialidades Carlos Andrade Marín; TIPS: Transyugular Porto Sistemic Shunt; CEISH: Comité de Ética en Investigación en Seres Humanos; IMB SPSS: Programa Estadístico International Business Machines / Statistical Package for the Social Sciences; IMC: Índice de Masa Corporal; LEUN: Lista de Espera Única Nacional; INDOT: Instituto Nacional de Donación y Trasplante de Órganos Tejidos y Células; MSP: Ministerio de Salud Pública del Ecuador; IESS: Instituto Ecuatoriano de Seguridad Social; ISSFA: Instituto de Seguridad Social de las Fuerza Armadas.
XA, JA, JP: Concepción y diseño del trabajo. SV, MF: Recolección y obtención de resultados. JA, JP: Análisis e interpretación de datos. XA, JA, SV, MF, JP: Redacción del manuscrito. JA, JR, JP: Revisión crítica del manuscrito. XA, JA, JR, JP: Aprobación de su versión final. JP: Asesoría estadística.
John Byron Abad González. Doctor en Medicina y Cirugía, Universidad de Guayaquil. Especialista en Cirugía General, Universidad Católica de Santiago de Guayaquil. Jefe de la Unidad Técnica de Trasplantes, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID ID: https://orcid.org/0000-0002-3637-291X
Nancy Jhoana Rivera Armijos. Doctor en Medicina y Cirugía, Especialista en Radiología e Imagen, Diploma superior en Gerencia de Servicios de Salud, Universidad Nacional de Loja. Médico General en Funciones Hospitalarias, Unidad Técnica de Imagenología, Hospital de Especialidades Carlos Andrade Marín. Quito- Ecuador ORCID ID: https://orcid.org/0000-0003-0516-1068
Ximena Alexandra Armijos Salinas. Doctor en Medicina y Cirugía, Diplomado Superior en Gerencia de Servicios de Salud, Universidad Nacional de Loja. Médico Especialista en Gastroenterología, Universidad del Salvador. Gastroenteróloga, Unidad Técnica de Gastroenterología, Hospital de Especialidades Carlos Andrade Marín. Quito- Ecuador ORCID ID: https://orcid.org/0000-0003-3732-0027
Stefanny Ibeth Viteri Ávila. Médico, Universidad Central del Ecuador. Magister en Salud y Seguridad Ocupacional Mención en Prevención de Riesgos Laborales, Universidad Particular Internacional SEK. Médico General en Funciones Hospitalarias, Unidad Técnica de Gestión de Trasplantes, Hospital de Especialidades Carlos Andrade Marín. Quito- Ecuador. ORCID ID: https://orcid.org/0000-0002-9923-9673
Santiago Jefferson Piedra Andrade. Médico, Universidad Central del Ecuador. Médico General en Funciones Hospitalarias, Unidad Técnica de Nefrología, Hospital de Especialidades Carlos Andrade Marín. Quito-Ecuador. ORCID ID: https://orcid.org/0000-0003-3003-065X
María José Fiallos Reinoso. Médica General, Universidad Nacional de Chimborazo. MEDIFRA Soluciones Médico Ocupacional Ecuador, Prevención en Riesgos Laborales. Médica General en Funciones Hospitalarias, Unidad Técnica de Gestión Hospitalaria, Hospital de Especialidades Carlos Andrade Marín. Quito- Ecuador. ORCID ID: https://orcid.org/0000-0002-6302-7038.
Se utilizaron recursos bibliográficos de uso libre y limitado. La información recolectada está disponible bajo requisición al autor principal.
El estudio fue aprobado por pares y por el Comité de Ética de Investigación en Seres Humanos CEISH-HCAM.
La publicación fue aprobada por el Comité de Política Editorial de la Revista Médica Científica CAMbios del HECAM en Acta 002 de fecha 29 de diciembre de 2020.
Se trabajó con recursos propios de los autores.
Los autores reportaron no tener ningún conflicto de interés personal, financiero, intelectual, económico y de interés corporativo.
A la Unidad Técnica de Trasplante Hepático del Hospital de Especialidades Carlos Andrade Marín. A la Dra. Gabriela Alexandra Mosquera Correa y Jenny Marghiory Erazo Mejía de la Coordinación General de Investigación por su colaboración para la publicación de la investigación.