CAMbios. 2024, v.23 (1): e939
1 Guadalupe Elizabeth Freire Ortiz
Hospital de Especialidades Carlos Andrade Marín, Unidad Técnica de Gastroenterología. Quito-Ecuador. Correo: lupita31freire@hotmail.com
ORCID https://orcid.org/0009-0007-9376-4286
2 María Monserrate Briceño Kirby
Instituto Ecuatoriano de Enfermedades Digestivas. Uni- dad Médica de Gastroenterología. Guayaquil – Ecuador. Correo: mmkirby@gmail.com
Correspondencia autor:
Nombre completo del autor corresponsal: Guadalupe
Elizabeth Freire Ortiz
Dirección del autor. Ciudad-País: Pedro Moncayo y Yaguachi. Quito – Ecuador.
Código postal:
170136
Teléfono: (593) 95122066
Copyright: ©HECAM
ESTUDIO ORIGINAL: ESTUDIO OBSERVACIONAL
Complicaciones, clínica y tratamiento
de pacientes con hepatocarcinoma,
posterior a quimioembolización en dos hospitales de Quito.
Complications, symptoms and treatment of patients with hepatocellular
carcinoma, after chemoembolization in two hospitals in Quito.
 Guadalupe Elizabeth Freire Ortiz 1, María Monserrate Briceño Kirby 2
Guadalupe Elizabeth Freire Ortiz 1, María Monserrate Briceño Kirby 2
Recibido: 21-11-2023 Aprobado: 23-05-2024
Publicado: 16-07-2024
RESUMEN
INTRODUCCIÓN. La
quimioembolización transarterial ha demostrado mejorar la tasa de so- brevida
en los pacientes con hepatocarcinoma, se ha descrito como tratamiento
paliativo; es útil, efectivo y bien tolerado.
Esta terapéutica tiene el objetivo de disminuir
el volumen tumo- ral.
OBJETIVO. Determinar las complicaciones que presentan los pacientes con diagnóstico
de hepatocarcinoma, posterior a la realización de quimioembolización
transarterial del servicio de Gastroenterología del Hospital de Especialidades Carlos Andrade Marín y Hospital
de Es- pecialidades Eugenio
Espejo, durante el período enero 2015 - enero 2020. MATERIALES Y MÉTODOS. Es un estudio retrospectivo observacional transversal; se
diseñó un formulario de recolección de información,
utilizando media y desvío estándar para variables cuantitativas;
frecuencia y porcentaje para cualitativas; en las variables con distribución no
paramétrico se recurrió a la mediana, rango intercuartil y sus intervalos, además se utilizó
Chi Cuadrado, Índice de Yates y test de U Mann Whitney. Se trabajó en el paquete
estadístico SPSS versión
26. RESULTADOS. Se analizaron 97 pacientes, el 60,8% fue de sexo masculino de los cuales el
56.7% presentó alguna comorbilidad; la mayoría de los pacientes no tuvieron
complicaciones, sin embargo, la hipertensión arterial
se presentó como manifestación
clínica post quimioembolización transarterial (10,3%); el choque, el síndrome
ascítico – edematoso y el dolor abdominal fueron
las complicaciones de mayor frecuencia. Los datos
estadísticamente significativos
fueron
los siguientes: los pacientes con hepatocarcinoma y cirrosis hepática con
severidad Child Pugh B, tuvieron un porcentaje mayor de complicaciones valor p
= 0,01; un tamaño más grande del tumor sobre el número de lesiones, se relacionó con presentar alguna complicación
postquimioembolización transarterial valor p = 0,001, lo
que significó un aumento en la estancia hospitalaria valor p = 0,006; los pacientes que presentaron complicaciones mayores y menores tuvieron un tiempo de
hospitalización más prolongado valor p < 0,05; la asociación entre la
mortalidad y las complicaciones post quimioembolización en hospitalización y en
UCI tuvieron una tasa general de 3,2% valor p = 0,001. CONCLUSIÓN. Las complicaciones mayores como el síndrome
ascítico edematoso y el estado de choque,
se mantuvieron sobre la media general.
Con una tasa de mortalidad esperada según la tendencia internacional.
Palabras clave: Escleroterapia;
Carcinoma Hepatocelular; Sobrevida; Hipertensión; Choque; Ascitis.
ABSTRACT
INTRODUCTION: Transarterial chemoembolization has been shown
to improve the survival rate in
patients with hepatocarcinoma, it has been described as palliative treatment; it is useful,
effective and well tolerated. This therapy aims to reduce tumor volume, due to its embolic, vascular and cytotoxic effects. OBJECTIVE: To determine
the complications presented
by patients diagnosed
with hepatocarcinoma, after performing transarterial chemoembolization of the Gastroenterology service
of the Carlos Andrade Marín Specialty Hospital
and Eugenio Espejo Specialty
Hospital, during the period January
2015 - January 2020. METHODOLOGY: This cross-sectional observational study was conducted
in patients with hepatocarcinoma who underwent transarterial chemoembolization. A form was designed for the collection of information, through a
pseudonymized database, which was analyzed
using the statistical package SPSS version
26.
RESULTS: 97
patients were analyzed, 60.8% were male, of which 56.7% presented some co-
morbidity; Most of the patients
had no complications, however, arterial
hypertension presented as a clinical
manifestation after transarterial chemoembolization in 10.3%; shock, ascites
edema decompensation and abdominal
pain were the most frequent
complications. The statistically
significant data
were the following: patients
with hepatocellular carcinoma
and liver cirrhosis with Child
Pugh B severity had a higher percentage of complications valor p = 0,01; a
larger tumor size compared to the number of lesions was related to presenting
some post-transarterial che- moembolization
complication valor p = 0,001,
which meant an increase in hospital stay valor p =
0,006; patients who presented major and minor complications had a longer
hospitalization time valor p < 0,05, the association between mortality and post chemoembolization complications in
hospitalization and in the ICU had an overall rate of 3.2% valor p = 0,001.
CONCLUSION. Major
complications, such as edematous ascitic syndrome and shock, remained above the
general average. With an expected mortality rate according to the international
trend.
Keywords: Sclerotherapy;
Carcinoma, Hepatocellular; Survival; Hypertension; Shock; Ascites.
CAMbios https://revistahcam.iess.gob.ec/index.php/cambios/issue/ archive
e-ISSN:
2661-6947
Periodicidad semestral: flujo continuo Vol.
23 (1) Ene-Jun 2024 revista.hcam@iess.gob.ec
DOI: https://doi.org/10.36015/cambios.v23.n1.2024.939
Esta obra está
bajo una licencia internacional Creative Commons
Atribución-NoComercial

.
INTRODUCCIÓN
La quimioembolización
transarterial (TACE) es
una opción
terapéutica, que se aplica
principalmente en el
manejo del he- patocarcinoma (CHC), sin embargo, también está indicada en pacientes con metástasis hepáticas
múltiples del cáncer
colorrectal, que no son
candidatos a resección, ablación o cirugía, tumores neuroendocrinos gastropancreáticos
y terapia puente para trasplante
hepático 1-3.
A nivel mundial el hepatocarcinoma es el 6to tumor más frecuente,
su incidencia
al año
es de
500 000
a 1 000 000 de casos y es la tercera causa de muerte por cáncer 4-6.
Las complicaciones de la TACE son
raras, con una frecuencia baja aproximadamente del 5% las
cuales en caso de presentarse
y no manejarlas de forma adecuada
pueden ser suma- mente graves con riesgo incluso de muerte 4,7-9.
El manejo
en las
unidades hospitalarias de nuestro medio
no siempre puede ser realizado de
acuerdo a los lineamientos in- ternacionales,
ya sea
por falta
de insumos
o personal calificado, siendo realizados dichos procedimientos con ciertas
limitaciones que pueden aumentar la
probabilidad de presentar complicaciones post intervención, de ahí la importancia de determinar si es un hecho estadísticamente relevante o no 10-13.
El trabajo
de investigación
tiene los siguientes objetivos: de- terminar las complicaciones
que presentan
los pacientes
con diagnóstico de CHC posterior a la realización de TACE, analizar la relación entre las características sociodemográficas
y clínicas con las complicaciones, identificar
el período de estancia hospitalaria
en complicaciones
mayores, menores y determinar la frecuencia
de mortalidad
posterior al procedimiento.
Además de
servir como base para el
desarrollo de trabajos científicos de mayor complejidad, una vez que se conozcan
las complicaciones más frecuentes
después de la
TACE, esta
información permitirá plantear la
posibilidad de actualizar los protocolos de manejo de las
dos unidades
de salud
que par- ticipan en el
estudio, para mejorar la atención del paciente y evitar una mayor morbi-mortalidad.
MATERIALES Y MÉTODOS
Se trata
de un
estudio retrospectivo observacional
transversal, la población está representada por los pacientes hospitalizados
con diagnóstico de hepatocarcinoma
sometidos a quimioembolización transarterial
del servicio
de Gastroenterología
en dos hospitales de Quito durante el período enero 2015 – enero 2020. Se tomó como muestra
a todos los pacientes con hepatocarcinoma sometidos a quimioembolización transarterial, se
analizaron 97 pacientes
durante el periodo de estudio.
Los criterios
de inclusión
fueron: historias clínicas de pacientes mayores de 18 años de edad hasta los 70 años de edad, de
ambos sexos con diagnóstico de hepatocarcinoma durante el período enero 2015 a enero
2020 e historias clínicas de pacientes cirróticos y no cirróticos
con diagnóstico de hepatocarcinoma
sometidos
a quimioembolización transarterial.
CIE-10: C22.9,
C22.0, D01.5, D37.6, K74.6. Los
pacientes fallecidos también fueron incluidos en este estudio.
Los
criterios de exclusión fueron: historias clínicas de pacientes
embarazadas con diagnóstico de hepatocarcinoma. CIE-10: O9A.1, O99.89, incongruencia o falta de datos en la historia
clí- nica e historias clínicas de pacientes con diagnóstico de hepatocarcinoma que no se encuentren durante el período enero 2015 a enero 2020.
Se diseñó
un formulario
para la recolección de información,
en la cual están contempladas todas las variables que se incluyó
en el estudio (Anexo 1. Formulario
de recolección). Se
tomó como sustento bibliográfico un estudio observacional retrospectivo realizado por Marcacuzco en el 201810. El acceso a la información se solicitó mediante un oficio la creación de un usuario para el ingreso a las historias
clínicas, que se encontraban debidamente anonimizadas.
El análisis
univariado se llevó a cabo con estadística descriptiva en la que se utilizó media y desvío estándar
para variables cuan-
titativas; frecuencia y porcentaje
para las variables cualitativas; en las variables con distribución
no paramétrico
se recurrió
a la mediana, rango intercuartil y sus intervalos.
Por su
parte, el análisis bivariado se
procedió a realizar con estadística inferencial previa dicotomización de algunas variables,
utilizando estadístico Chi Cuadrado y en caso de frecuencias esperadas menores a 5, a su ajuste con Índice de Yates; para el contraste de
hipótesis entre variables cuantitativas y cualitativas se utilizó el test de U Mann Whitney, para todo ello se planteó un nivel
de valor p de significancia de menor a 0,05. Se trabajó en el paquete estadístico SPSS versión 26.
RESULTADOS
En total se analizaron
97 pacientes, el sexo masculino representó
el 60,8%, de los
cuales el 56.7% presentó alguna
comorbilidad. La etiología más frecuente del CHC fue la desconocida y la metabólica en el 28,9% y 25,8
% respectivamente. El 69.1%
no tuvo antecedentes de
TACE y el 82.5% presentó cirrosis hepática subyacente.
Los pacientes
con hepatocarcinoma
y hepatopatía crónica en
estadio cirrótico con severidad
Child Pugh B, tuvieron un porcentaje mayor de complicaciones, lo cual fue estadísticamente significativo. El 77,7% de los pacientes con estadiaje BCLC A se complicó
(Tabla 1).
 Tabla 1. Relación
entre las complicaciones post quimioembolización transarterial y las variables
sociodemográficas y clínicas.
Tabla 1. Relación
entre las complicaciones post quimioembolización transarterial y las variables
sociodemográficas y clínicas.
Complicación post TACE
Total Valor p
|
|
Si
12 (%)
|
No
85 (%)
|
97 (%)
|
|
|
Sexo
|
Femenino
|
6 (50)
|
32 (37,6)
|
38 (39,2)
|
0,41
|
|
|
Masculino
|
6 (50)
|
53 (62,4)
|
59 (60,8)
|
|
|
Comorbilidades
|
Si
|
5 (41,7)
|
50 (58,8)
|
55 (56,7)
|
0,26
|
|
|
No
|
7 (58,3)
|
35 (41,2)
|
42 (43,3)
|
|
|
Etiología
|
Alcohol
|
3 (25)
|
14 (16,5)
|
17 (17,5)
|
0,9
|
|
|
Autoinmune
|
0 (0)
|
1 (1,2)
|
1 (1)
|
|
|
|
Desconocida
|
2 (16,7)
|
26 (30,6)
|
28 (28,9)
|
|
|
|
Metabólica
|
3 (25)
|
22 (25,9)
|
25 (25,8)
|
|
|
|
No cirrótico
|
3 (25)
|
15 (17,6)
|
18 (18,6)
|
|
|
|
VHB
|
1 (8,3)
|
7 (8,2)
|
8 (8,2)
|
|
|
Antecedente de TACE
|
Si
|
1 (8,3)
|
29 (34,1)
|
30 (30,9)
|
0,07
|
|
|
No
|
11 (91,7)
|
56 (65,9)
|
67 (69,1)
|
|
|
Cirrosis hepática
|
Si
|
9 (75)
|
71 (83,5)
|
80 (82,5)
|
0,46
|
|
|
No
|
3 (25)
|
14 (16,5)
|
17 (17,5)
|
|
|
Child-Pugh
|
A
|
2 (22,2%)
|
47 (66,2%)
|
49 (61,3%)
|
0,01*
|
|
|
B
|
7 (77,7%)
|
24 (33,8%)
|
31 (38,8%)
|
|
|
|
Total
|
9 (100%)
|
71 (100%)
|
80 (100%)
|
|
|
Estadiaje BCLC
|
A
|
7 (77,7%)
|
60 (84,5%)
|
67 (83,8%)
|
0,6
|
|
|
B
|
2 (22,2%)
|
11 (15,5%)
|
13 (16,3%)
|
|
|

|
Total
|
9 (100%)
|
71 (100%)
|
80 (100%)
|
|
*Estadísticamente significativo: p < 0,05, chi cuadrado.
Fuente: base de datos HCAM y HEEE
Elaboración: Freire G, Briceño M
Se puede
observar que la muestra se
caracterizó por tener pacientes con
una edad
promedio de 70 años, cuyo
tamaño del tumor tuvo un valor promedio
de 5 cm (Tabla 2).
 Tabla 2. Caracterización estadística de la edad
y el tamaño del tumor en pacientes
con diagnóstico de hepatocarcinoma sometidos a quimioembolización transarterial.
Tabla 2. Caracterización estadística de la edad
y el tamaño del tumor en pacientes
con diagnóstico de hepatocarcinoma sometidos a quimioembolización transarterial.
 Variable Mínimo
Máximo
Mediana*
RIQ
Edad (años)
Variable Mínimo
Máximo
Mediana*
RIQ
Edad (años)
28 86 70
33 – 72
 Tamaño del tumor (cm)
0,1
20
5 4,5 – 16
Tamaño del tumor (cm)
0,1
20
5 4,5 – 16
Fuente: base de datos HCAM y HEEE
Elaboración: Freire G, Briceño M.
Un
tamaño más grande del tumor sobre el número de lesiones, se
relacionaron con presentar
alguna complicación postquimioembolización transarterial, lo que significó
un aumento en la estancia
hospitalaria (Tabla 3).
Tabla 3. Relación entre
las
complicaciones
post
quimioembolización
transarterial con el tamaño del tumor, el número de lesiones
y los días de
hospitalización

 Variable Complicación post TACE Valor p
Variable Complicación post TACE Valor p
Si No
Tamaño del tumor (cm)
9 4 0,001*
|
Número de lesiones
|
1
|
1
|
0,488
|
|
Días de hospitalización
|
6,5
|
4
|
0,006*
|
*Estadísticamente significativo: p ≤ 0,05, estadístico: U Mann Whitney
Fuente: base de datos HCAM y HEEE
Elaboración: Freire G, Briceño M.
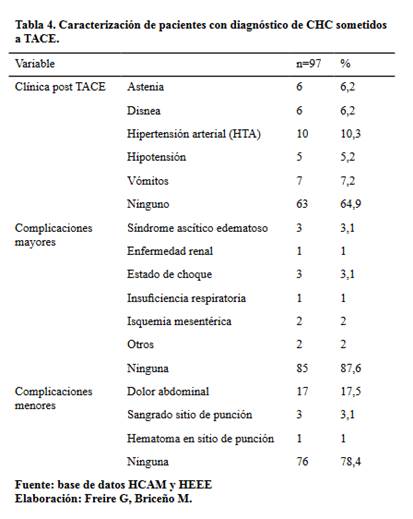
La mayor parte de los pacientes
no presentaron complicaciones,
sin embargo,
aquellos que las presentaron entre las más frecuentes fueron: clínica post TACE, la HTA en el 10.3%; complicaciones mayores: el síndrome ascítico edematoso y el estado de choque
en el 3.1%; complicaciones menores: el dolor abdominal en el 17% (Tabla 4).
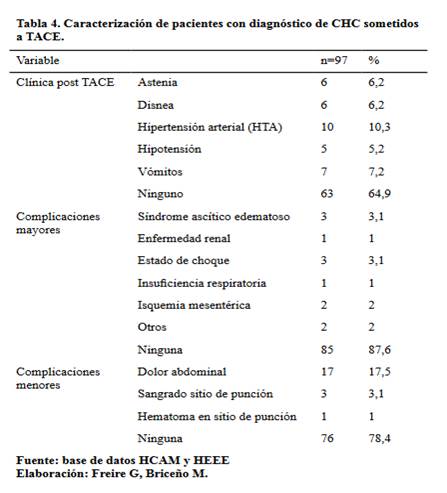
En pacientes con
antecedentes de cirrosis hepática el 11.13% presentó alguna complicación mayor
y el 20% una complicación menor, mientras que, los pacientes
no cirróticos,
en el
17,6% se expresó una complicación mayor y en el 29,4%
una complicación menor, sin embargo, estas diferencias no fueron estadísticamente
significativas (Tabla 5).
Los pacientes tuvieron
una estancia hospitalaria promedio de 6.5 días para
complicaciones mayores y 6 días para
complicaciones menores, a diferencia
de los que no presentaron ninguna complicación, tuvieron un período de hospitalización de 4 días (Tabla 6).
Tabla
6. Días de estancia hospitalaria en complicaciones mayores y menores, pacientes
con Hepatocarcinoma,
posterior
a la realización de Quimioembolización transarterial.
______________________________________________________________________________________________
Días de
hospitalización Valor
p
______________________________________________________________________________________________
Complicación mayor Si 6,5 *0,006
No 4
Complicación menor Si 6 *0,01
No 4
______________________________________________________________________________________________
*Estadísticamente
significativo: p ≤ 0,05, estadístico: U Mann Whitney
Fuente: base de datos HCAM y
HEEE
Elaboración: Freire G, Briceño
M
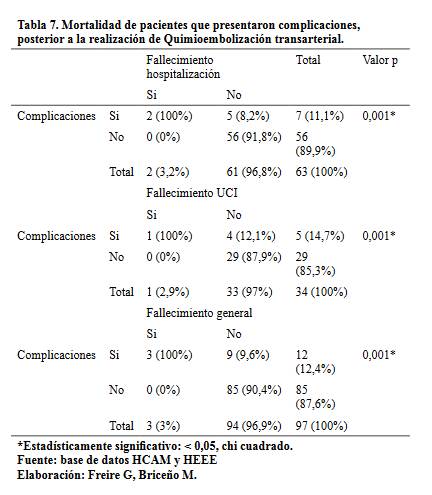
Se puede apreciar que la
asociación entre mortalidad y complicaciones post TACE en hospitalización fue
del 3,2% y en UCI del 2,9%; con una tasa general de 3,2% dicha relación fue
estadísticamente significativa (Tabla 7).
DISCUSIÓN
En relación con las
características del tumor, el tamaño promedio del CHC fue de 5cm, a diferencia
de otra publicación en donde el diámetro tumoral fue menor; el tamaño tumoral
es importante ya que los pacientes con CHC menores a 5 cm de diámetro posterior
a realizarse TACE, presentan un mayor período libre de enfermedad y una mayor
respuesta al tratamiento, de igual manera se observó que los pacientes
cirróticos con un estadio Child B, presentaron más complicaciones, estos datos tienen
similitud al estudio de Hatanaka que valoró la severidad de la cirrosis
hepática14-16.
Se observó que los pacientes
tuvieron una estancia hospitalaria de alrededor de 6 días en promedio, tanto
para las complicaciones mayores y menores; en un estudio publicado por Marcacuzco
manifiesta que el período de hospitalización depende del tipo de complicaciones
que presenten los pacientes posteriores al procedimiento, siendo así, según
esta publicación para el síndrome post TACE, el período de estancia
hospitalaria puede prolongarse hasta 10 días10
La tasa de mortalidad
relacionada con el procedimiento fue baja, datos similares a los estudios internacionales,
entre ellos, el estudio de Hanataka describe que la mortalidad fue menor a
1.5%, este hecho se presentó en pacientes con diagnóstico de bilioma que
ameritaron drenaje transhepático percutáneo16-20.
CONCLUSIONES
• Las complicaciones mayores, más frecuentes fueron el síndrome ascítico – edematoso
y el estado de shock, mientras que dentro de las complicaciones menores principalmente
se encuentra el dolor abdominal.
• El
tiempo de estancia hospitalaria para los pacientes que
presentaron complicaciones mayores fue
de 6,5
días y para los pacientes que presentaron
complicaciones menores fue
de 6 días.
• La tasa de mortalidad
general de los pacientes post
TACE
fue del 3.2%, similar
a lo evidenciado en la bibliografía
internacional.
ABREVIATURAS
MELD: Model For End - Stage Liver Disease
CHC: carcinoma hepatocelular
TACE: Quimioembolización transarterial
UCI: Unidad de Cuidados
Intensivos
HECAM: Hospital
de Especialidades Carlos Andrade Marín
CEISH: Comité de Ética de Investigación en Seres Humanos
CONTRIBUCIÓN DE LOS
AUTORES
Concepción y diseño
del trabajo.
GF y MB: Recolección de datos
y obtención de resultados. GF y MB: Análisis
e interpretación de datos. GF
y MB: Redacción del manuscrito. EC:
Revisión crítica del manuscrito. EC: Aprobación de su versión final.
GF y MB: Aporte de pacientes o material
de estudio. GF y MB: Obtención de financiamiento.
GF
Y MB: Asesoría estadística. GF Y MB: Asesoría técnica
o administrativa. GF y MB:
Rendición de cuentas (ICMJE). GF
y MB: Otras contribuciones (material
didáctico).
DISPONIBILIDAD DE DATOS Y MATERIALES
Se utilizaron
recursos bibliográficos de uso libre y limitado.
La información recolectada está disponible bajo requisición al autor
principal.
APROBACIÓN DEL COMITÉ DE ÉTICA Y CONSENTIMIENTO PARA PARTICIPAR EN EL ESTUDIO
El estudio
fue aprobado
por pares
por el
Comité de Ética de Investigación en Seres Humanos – CEISH HECAM. y del Departamento de
Docencia del Hospital de
Especialidades Eugenio Espejo.
CONSENTIMIENTO PARA PUBLICACIÓN
La
publicación fue aprobada
por el Comité
de
Política Editorial de la Revista Médico
Científica CAMbios
del HECAM en Acta 003
de fecha 23 de mayo de 2024.
FINANCIAMIENTO
Se trabajó con recursos
propios de los autores.
CONFLICTOS DE INTERÉS
Los autores reportaron
no tener ningún conflicto de interés, personal, financiero,
intelectual, económico y de interés corporativo.
REFERENCIAS BIBLIOGRÁFICAS
1.
Cheng Z, Lei Z, Jin X, Zhang Q, Si A, Yang P, et al. Postoperative adjuvant transarterial chemoembolization for intrahepatic
cholangiocarcinoma
patients
with
microvascular invasion: a propensity
score analysis. Journal of Gastrointestinal Oncology [Internet]. 2021 Apr 1 [cited 2022 Feb
7];12(2):819–30. doi: 10.21037/jgo-20-443.
Available from: https://pubmed.ncbi.nlm.nih.gov/34012669/
2. Nishida K, Lefor AK, Funabiki T. Rupture of Hepatocellular Carcinoma after Transarterial Chemoembolization followed by Massive Gastric Bleeding. Case Reports Hepatol.
2018 Jun 4;2018:4576276. doi: 10.1155/2018/4576276.
PMID: 29974003; PMCID: PMC6008880. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6008880/
3. Piscoya, A., Atamari-Anahui, N., Ccorahua-Rios, M. S., & Parra del Riego, A.
Tendencia
nacional de la mortalidad por hepatocarcinoma registrada en el Ministerio de Salud del Perú del 2005 al 2016. Acta gastroenterológica
Latinoamericana. 2020: 50(3). DOI://doi.org/10.52787/irgi9687.
Disponible
en:
https://actagastro.org/tendencia-nacional-de-la-mortalidad-por-hepatocarcinoma-regis- trada-en-el-ministerio-de-salud-del-peru-del-2005-al-2016/
4. García Pacheco
AV, Dajaro Castro LA, Bermeo Ortega JC,
Benalcázar Decker GN. Transarterial chemoembolization in
atypical hepatocellular carcinoma. Revista Virtual de la So- ciedad Paraguaya de Medicina Interna. 2018 Sep 30 [cited 2022 Feb 7];5(2):89–94.
Available from: https://dialnet.unirioja.es/servlet/articulo?codigo=6608300
5. Armengol, C., Sarrias, M. R., & Sala, M. (2018). Carci- noma hepatocelular: presente y futuro. Medicina
clínica, 150(10), 390–397. DOI:
10.1016/j.medcli.2017.08.010. Disponible
en: https://www.sciencedirect.com/science/article/abs/pii/S0025775317307170?via%3Dihub
6. Chang Y, Jeong SW, Young Jang J, Jae Kim Y. Recent Up- dates of Transarterial Chemoembolization in Hepatocellular
Carcinoma. International Journal of
Molecular Sciences [Internet]. 2020 Jan 1 [cited 2022 Feb 7];21(21):8165. DOI: 10.3390/ijms21218165.
Available from: https://pubmed.
ncbi.nlm.nih.gov/33142892/
7. Reig, M., Forner, A., Ávila, M. A., Ayuso, C., Mínguez, B. (2021). Diagnóstico y tratamiento del carcinoma hepa- tocelular. Actualización del documento de consenso de la AEEH, AEC, SEOM, SERAM, SERVEI y SETH. Medicina Clínica, 156(9), 463.e1-463.e30.
https://doi.org/10.1016/j. medcli.2020.09.022.
Disponible en: https://www.science- direct.com/science/article/pii/S0025775320307697?via%-3Dihub
8. Renne SL, Sarcognato
S, Sacchi D, Guido M, Roncalli
M, Terracciano L, Di Tommaso L. Hepatocellular carci- noma: a clinical and pathological overview. Pathologica. 2021 Jun;113(3):203-217. PMID: 34294938; PMCID: PMC8299323. Available from: https://www.ncbi.nlm.nih. gov/pmc/articles/PMC8299323/
9. Schwartz,
J. M.,
Carithers, R. L., Sirlin, C.
B. Clinical
features and diagnosis of
hepatocellular carcinoma. UpTo- Date.
Disponble en: https://www.uptodate.com/contents/ clinical-features-and-diagnosis-of-hepatocellular-carcino-
ma?search=HEPATOCARCINOMA&source=search_re-
sult&selectedTitle=2~150&usage_type=default&display_
rank=2
10. Marcacuzco A, Nutu O-A, San Román Manso R, Justo Alonso I, Calvo Pulido J, Manrique Municio A, et al. Com-
plicaciones de la quimioembolización transarterial (QETA) en el tratamiento de los tumores hepáticos. Cirugía Española.
2018 Nov;96(9):560–7. DOI:10.1016/j.ciresp.2018.06.004. Disponible
en: https://www.sciencedirect.com/science/ar- ticle/abs/pii/S0009739X18301726?via%3Dihub
11. The Global Cancer Observatory. Globacan. Ecuador. The International Agency for Research on Cancer, OMS. 2022. Available from:
https://gco.iarc.who.int/media/globocan/
factsheets/populations/218-ecuador-fact-sheet.pdf
12. Villanueva
A. Hepatocellular Carcinoma. N Engl J
Med.
2019 Apr 11;380(15):1450-1462. DOI: 10.1056/
NEJMra1713263. PMID: 30970190. Available from: https://pubmed.ncbi.nlm.nih.gov/30970190/
13. Abdalla
E, Stuart K.
Descripción general de los enfoques de tratamiento para el carcinoma hepatocelular. UptoDate. 2021. Disponible
en: Acceso restringido con contraseña.
14. Curley S, Barnett C, Abdalla E. Management of potentially
resectable hepatocellular carcinoma:
Prognosis, role of neoadjuvant and adjuvant therapy, and posttreatment sur- veillance. UptoDate. 2021. Available
from: https://www.uptodate.com/contents/management-of-potentially-resectable-hepatocellular-carcinoma-prognosis-role-of-neoadju-
vant-and-adjuvant-therapy-and-posttreatment-surveillance
15. Jiménez LM, Rodriguez-Chavez A, Ramírez-Flores JL, Rodriguez-Villa
P, Jiménez-Partida
MÁ, Cervantes-Rodríguez G, et al. Manejo del hepatocarcinoma con celecoxib
y pentoxifilina: reporte
de un
caso. Revista Médica del Instituto
Mexicano del Seguro Social, 2018:
56(3), 309–315. Disponible en:
https://www.medigraphic.com/cgi-bin/new/
resumen.cgi?IDARTICULO=84084
16. Hatanaka
T, Arai H, Shibasaki
M, Tojima H, Takizawa
D, Toyoda M, Takayama H, et al. Factors predicting overall
response and overall survival
in hepatocellular
carcinoma patients undergoing balloon-occluded
transcatheter arterial chemoembolization: A retrospective cohort study. Hepatology
research : the official journal of the Japan Society of
Hepatology, 2018: 48(2),
165–175. DOI: doi.org/10.1111/
hepr.12912. Available from: https://pubmed.ncbi.nlm.nih. gov/28500686/
17. Bilbao JI, Páramo M, Madrid JM, Benito A. Hepatoce-
llular carcinoma treatment: ablation and
arterial embolization. Radiologia (Engl
Ed). 2018 Mar-Apr;60(2):156-166.
English, Spanish. DOI: 10.1016/j.rx.2017.09.004. Epub 2017 Nov 4. PMID: 29108656. Available
from: https://
pubmed.ncbi.nlm.nih.gov/29108656/
18. Zersenay A, Murray TE, Egri C, Chung J, Liu D, Elsayes
KM, et al.Treatment
response assessment following transarterial
radioembolization for hepatocellular
carcinoma. Radiología abdominal,
2021: 46(8), 3596–3614. DOI:10.1007/
s00261-021-03095-8. Available
from: https://link.springer. com/article/10.1007/s00261-021-03095-8
19.
Reig M, Forner A, Rimola J, Ferrer-Fàbrega J, Burrel M,
Garcia-Criado Á, et al.
BCLC strategy for
prognosis pre- diction and treatment recommendation: The 2022 update.
J Hepatol. 2022 Mar;76(3):681-693.
DOI: 10.1016/j. jhep.2021.11.018. Epub
2021 Nov 19. PMID: 34801630;
PMCID: PMC8866082. Available from:
https://pubmed. ncbi.nlm.nih.gov/34801630/
20.
Abad JB, Galarza DP, Chong RJ, Guerrero
FM, Viteri SI, Piedra
JS. Trasplante Hepático: Supervivencia global en el
Hospital de Especialidades Carlos Andrade Marín. Cambios
rev. méd. 2020; 19(2): 6-11.
Disponible en: https://revista- hcam.iess.gob.ec/index.php/cambios/article/view/657/374
![]() Guadalupe Elizabeth Freire Ortiz 1, María Monserrate Briceño Kirby 2
Guadalupe Elizabeth Freire Ortiz 1, María Monserrate Briceño Kirby 2